Sølv og svovlsyre:Forstå reaktionen (eller mangel på samme)
* Sølvs position i Reactivity Series: Sølv er et mindre reaktivt metal sammenlignet med brint. Det sidder under brint i reaktivitetsserien. Dette betyder, at det er mindre tilbøjeligt til at fortrænge brint fra dets forbindelser, herunder svovlsyre.
* Danning af et beskyttende lag: Når sølv kommer i kontakt med svovlsyre, dannes et tyndt lag sølvsulfat (Ag₂SO4) på dets overflade. Dette lag fungerer som en beskyttende barriere, der forhindrer yderligere reaktion.
Der er dog nogle forhold, hvorunder sølv kan reagere med svovlsyre:
* Varm, koncentreret svovlsyre: Hvis du bruger varm, koncentreret svovlsyre, er reaktionen mulig. Den høje temperatur og den koncentrerede syre kan overvinde det beskyttende lag og føre til dannelsen af sølvsulfat og svovldioxid (SO₂).
* Tilstedeværelse af oxidationsmidler: Hvis du tilføjer et oxidationsmiddel, som salpetersyre, til svovlsyren, kan det hjælpe med at oxidere sølvet og fremme reaktionen. Dette skyldes, at oxidationsmidlet letter fjernelse af elektroner fra sølv, hvilket gør det mere sandsynligt, at det reagerer.
Den samlede reaktion med varm, koncentreret svovlsyre kan repræsenteres som:
2Ag(s) + 2H2SO4(l) → Ag2SO4(s) + SO2(g) + 2H2O(l)
Det er vigtigt at bemærke, at:
* Sølv reagerer med svovlsyre meget langsommere sammenlignet med reaktionen af mere reaktive metaller.
* Reaktionen kræver særlige forhold, hvilket gør den mindre almindelig i hverdagen.
Sig til, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
 Anisotrope plasmoner i kvasi-metalliske 2-D materialerFigur viser (til venstre) en visuel repræsentation af det melleminfrarøde anisotropiske plasmon i kvasi-metalliske fase 2D-TMDer. (Mellem) Kvasi-metallisk fase monolag-wolfram diselenid (WSe2) med det
Anisotrope plasmoner i kvasi-metalliske 2-D materialerFigur viser (til venstre) en visuel repræsentation af det melleminfrarøde anisotropiske plasmon i kvasi-metalliske fase 2D-TMDer. (Mellem) Kvasi-metallisk fase monolag-wolfram diselenid (WSe2) med det -
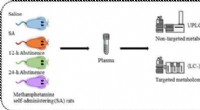 En rottehjerne, til og fra metamfetaminKredit:American Chemical Society Stofmisbrug er en ond cirkel af belønning og tilbagetrækning. Kroniske brugere får ofte tilbagefald på grund af de ubehagelige fysiske og psykiske symptomer, de op
En rottehjerne, til og fra metamfetaminKredit:American Chemical Society Stofmisbrug er en ond cirkel af belønning og tilbagetrækning. Kroniske brugere får ofte tilbagefald på grund af de ubehagelige fysiske og psykiske symptomer, de op -
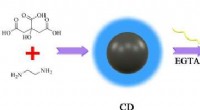 Kulstofprikker gør calcium lettere at sporeIllustration af Ca2+ -detektering ved hjælp af EGTA-modificerede cder. Kredit:SIBET På hospitaler, læger råder ofte patienter til at tage calciumtilskud. Men kommer calcium ind i de celler, der ha
Kulstofprikker gør calcium lettere at sporeIllustration af Ca2+ -detektering ved hjælp af EGTA-modificerede cder. Kredit:SIBET På hospitaler, læger råder ofte patienter til at tage calciumtilskud. Men kommer calcium ind i de celler, der ha -
 Sådan beregnes mol i en kemisk reaktion - Trin-for-trin-vejledningAf Kylene Arnold – Opdateret 30. august 2022 TL;DR For at bestemme mol i en reaktion skal du konvertere alle reaktantmasser til gram, beregne hver forbindelses molære masse, dividere gram med molær m
Sådan beregnes mol i en kemisk reaktion - Trin-for-trin-vejledningAf Kylene Arnold – Opdateret 30. august 2022 TL;DR For at bestemme mol i en reaktion skal du konvertere alle reaktantmasser til gram, beregne hver forbindelses molære masse, dividere gram med molær m
- Hvad har stjernerne at gøre med atomenergi?
- Bakteriefabrikker bruges til at opdage potentielle nye malariamedicin
- Hvad er skyer, der skaber torden- og lynstorm-tornadoer?
- Hvilket stof modstår ændringer i pH-niveauer?
- Undersøgelse foreslår, hvordan man bygger en bedre 'nanopore' biosensor
- 30-årig stjerneundersøgelse afslører mysterier om galaksers gigantiske planeter


