Fluors periodiske system nabo:Opdag chlors ligheder
Her er hvorfor:
* De er begge halogener: De tilhører gruppe 17 (VIIA) i det periodiske system, også kendt som halogenerne.
* Lignende elektronegativitet: Både fluor og klor har meget høj elektronegativitet, hvilket betyder, at de stærkt tiltrækker elektroner.
* Reaktive ikke-metaller: De er begge meget reaktive ikke-metaller, der let danner negative ioner (anioner).
* Lignende bindingsegenskaber: De har tendens til at danne enkelt kovalente bindinger med andre grundstoffer.
Der er dog nogle forskelle mellem de to:
* Fluor er det mest elektronegative grundstof: Det har en højere elektronegativitet end klor.
* Reaktivitet: Fluor er generelt mere reaktivt end klor.
* Atomstørrelse: Klor er større end fluor.
På grund af deres lignende elektronkonfigurationer og position i det periodiske system deler fluor og klor i det hele taget mange nøgleegenskaber.
 Varme artikler
Varme artikler
-
 Aktiv læring fremskynder redox-flow batteri opdagelseSømløse interaktioner mellem kvantemekaniske simuleringer og kunstig intelligens kunne give en effektiv materialeopdagelsesplatform. Kredit:Rajeev Surendran Assary / Argonne National Laboratory Ve
Aktiv læring fremskynder redox-flow batteri opdagelseSømløse interaktioner mellem kvantemekaniske simuleringer og kunstig intelligens kunne give en effektiv materialeopdagelsesplatform. Kredit:Rajeev Surendran Assary / Argonne National Laboratory Ve -
 Laser spor terapi, næringsstoffer, toksinerI biologiske systemer, kulstof-14 kan bruges som et biokemisk sporstof til at spore mikrodoser af næringsstoffer, toksiner og terapeutika hos mennesker og dyr. Kredit:Lawrence Livermore National Labor
Laser spor terapi, næringsstoffer, toksinerI biologiske systemer, kulstof-14 kan bruges som et biokemisk sporstof til at spore mikrodoser af næringsstoffer, toksiner og terapeutika hos mennesker og dyr. Kredit:Lawrence Livermore National Labor -
 Hvilken svejser er bedst til aluminium? TIG, MIG og fakkel forklaretAf Susan Kristoff, Opdateret 24. marts 2022 Aluminiumslegeringer udgør en unik udfordring sammenlignet med stål. Deres lavere smeltepunkt og højere varmeledningsevne kan forårsage gennembrænding, isæ
Hvilken svejser er bedst til aluminium? TIG, MIG og fakkel forklaretAf Susan Kristoff, Opdateret 24. marts 2022 Aluminiumslegeringer udgør en unik udfordring sammenlignet med stål. Deres lavere smeltepunkt og højere varmeledningsevne kan forårsage gennembrænding, isæ -
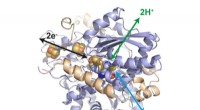 Enzymsystem til brintindustrienStruktur af hydrogenasen fra Desulfovibrio desulfuricans. I sit aktive center, en jern-svovl-klynge katalyserer oxidation af hydrogen til protoner samt reduktion af protoner til hydrogen. Yderligere j
Enzymsystem til brintindustrienStruktur af hydrogenasen fra Desulfovibrio desulfuricans. I sit aktive center, en jern-svovl-klynge katalyserer oxidation af hydrogen til protoner samt reduktion af protoner til hydrogen. Yderligere j
- Hvad er en tiende millimeter?
- Hvor synker den oceaniske skorpe ned i mantel?
- En million planter og dyr er på randen af udryddelse, og du kan sandsynligvis gætte, hvem der sk…
- Hvad er flasken lavet af?
- Løsning af mangeårige mysterier om de første parallakser i astronomi
- Husets efterretningschef siger, at Facebook arbejder på valgtrusler


