Enzymsystem til brintindustrien
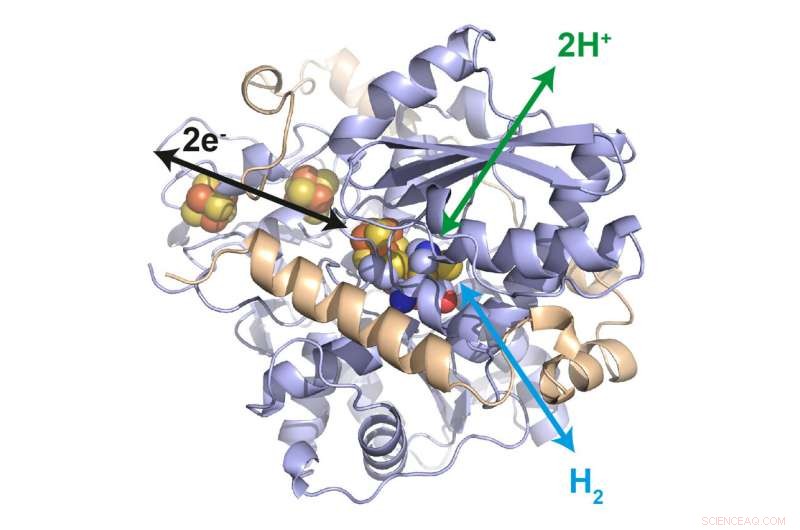
Struktur af hydrogenasen fra Desulfovibrio desulfuricans. I sit aktive center, en jern-svovl-klynge katalyserer oxidation af hydrogen til protoner samt reduktion af protoner til hydrogen. Yderligere jern-svovlklynger muliggør elektronoverførsel til den omgivende polymer. Kredit:Dr. James Birrell / MPI CEC
Et enzym kan gøre en drøm til virkelighed for energiindustrien:Det kan effektivt producere brint ved hjælp af elektricitet og kan også generere elektricitet fra brint. Enzymet beskyttes ved at indlejre det i en polymer. Et internationalt forskerhold med betydelig deltagelse af forskere fra Münchens tekniske universitet (TUM) har præsenteret systemet i det anerkendte videnskabstidsskrift Naturkatalyse .
Brændselsceller omdanner brint til elektricitet, mens elektrolysatorer bruger elektricitet til at splitte vand til at producere brint. Begge har brug for den sjældne og dermed dyre ædelmetalplatine som katalysator. Naturen har skabt en anden løsning:Enzymer, kaldet hydrogenaser. De katalyserer omdannelsen af brint meget hurtigt og næsten uden energitab.
Imidlertid, tidligere blev disse biokatalysatorer ikke anset for egnede til industriel brug på grund af deres høje følsomhed over for ilt. Nu et forskerhold fra det tekniske universitet i München (TUM), Ruhr-Universität Bochum (RUB), Det er lykkedes det franske nationale center for videnskabelig forskning (CNRS) i Marseille og Max-Planck Institute for Chemical Energy Conversion at integrere de følsomme enzymer i en beskyttende polymer på en måde, der gør dem levedygtige til brug ved teknisk brintomdannelse.
Holdbarhed vs. aktivitet
"Når de følsomme hydrogenaser er indlejret i egnede polymerer, fortsætter de med at virke i flere uger, selv i nærvær af ilt, "siger Nicolas Plumeré, Professor for elektrobioteknologi på TUM Campus Straubing for bioteknologi og bæredygtighed. "Uden denne beskyttelse mister de deres aktivitet inden for få minutter."
Indlejring af hydrogenaser i polymerer, hvis sidekæder kan overføre elektroner, kaldet redoxpolymerer, har ikke desto mindre to afgørende ulemper:et højt modstandsniveau modvirker elektronstrømmen gennem redoxpolymeren. Dette kræver investering af energi, som derefter går tabt i form af varme. Og de indlejrede hydrogenaser mister fuldstændigt deres evne til at generere brint.
Finjusteringspotentiale
Med et smart udvalg af de rigtige polymersidekæder, det er nu lykkedes forskerteamet at indstille polymerens redoxpotentiale på en sådan måde, at kun en lille overspænding er nødvendig for at overvinde modstanden.
Mere detaljerede undersøgelser afslørede derefter, at potentialet for sidekæderne var flyttet lidt til positive værdier på grund af indlejringen i polymermatrixen. I et yderligere forsøg brugte de en sidekæde med et tilsvarende negativt potentiale. Dette trick var gennembruddet:Hydrogenasen var nu i stand til at katalysere reaktionen i begge retninger uden energitab.
Biokatalysator til brintomdannelse
Ved hjælp af dette system byggede forskergruppen derefter en brændselscelle, hvor ilt reduceres af enzymet bilirubinoxidase fra bakterien Myrothecium verrucaria, mens hydrogenasen indlejret i polymerfilmen oxiderer hydrogenet fra bakterien desulfovibrio desulfuricans, producerer elektricitet i processen.
Cellen opnåede en værdi, med en åben kredsløbsspænding på 1,16 V, den højeste nogensinde målt for et system af denne type og tæt på det termodynamiske maksimum. Med tre milliamper per kvadratcentimeter opnåede cellen en meget høj effekttæthed for biologiske celler på samme tid.
Systemet kan også bruges til omvendt reaktion, producerer brint ved at forbruge elektroner:Energiomdannelseseffektiviteten er tæt på 100 procent, selv med effekttætheder på over fire milliamper per kvadratcentimeter.
Blueprint til nye biokatalysatorer
"Reduktionen af energitab har to afgørende fordele, "siger Nicolas Plumeré." Først, det gør systemet væsentligt mere effektivt; sekund, varmen, der genereres i en brændselscellestabel ved høje ydelsesniveauer, ville udgøre et problem for biologiske systemer. "
For at gøre deres system konkurrencedygtigt med systemer, der anvender platinbaserede katalysatorer, teamets igangværende forskning er nu fokuseret på at forbedre stabiliteten af hydrogenaserne ved højere effekttætheder.
Desuden, fundene kan også overføres til andre meget aktive, men følsomme katalysatorer til energiomdannelse og elektrosyntese. Direkte mål her er primært kuldioxidreducerende enzymer, der kan bruge elektricitet til at producere flydende brændstoffer eller mellemprodukter fra kuldioxid.
 Varme artikler
Varme artikler
-
 Spyt kan påvirke smagspræferencerSpyt opsamlet før og efter smagning af chokolademælkprøver analyseres for ændringer i proteiner, der kan påvirke bitterheden. Kredit:Cordelia Running Spyt er afgørende for at smage og fordøje mad,
Spyt kan påvirke smagspræferencerSpyt opsamlet før og efter smagning af chokolademælkprøver analyseres for ændringer i proteiner, der kan påvirke bitterheden. Kredit:Cordelia Running Spyt er afgørende for at smage og fordøje mad, -
 Kemikere udvider den genetiske kode for E. coli til at producere den 21. aminosyre, giver det nye ev…Forskere fra Rice University introducerede ikke -kanoniske aminosyre byggesten i proteiner i levende celler, banebrydende et kraftfuldt værktøj til at undersøge og manipulere proteiners struktur og fu
Kemikere udvider den genetiske kode for E. coli til at producere den 21. aminosyre, giver det nye ev…Forskere fra Rice University introducerede ikke -kanoniske aminosyre byggesten i proteiner i levende celler, banebrydende et kraftfuldt værktøj til at undersøge og manipulere proteiners struktur og fu -
 Simulering af AsqJ-enzymet åbner op for nye muligheder for farmaceutisk kemiMens forskellen mellem den naturlige og den modificerede AsqJ kun er én aminosyre, reaktiviteten er klart anderledes. Den naturlige AsqJ (venstre) har en valin i position 72 (blå). Den modificerede fo
Simulering af AsqJ-enzymet åbner op for nye muligheder for farmaceutisk kemiMens forskellen mellem den naturlige og den modificerede AsqJ kun er én aminosyre, reaktiviteten er klart anderledes. Den naturlige AsqJ (venstre) har en valin i position 72 (blå). Den modificerede fo -
 Forskere opdager ny type selvhelbredende materialeØverste panel:Optiske mikroskopbilleder af beskadigede (venstre) og reparerede (højre) prøver af et af materialerne i luft ved 25 °C. En film blev knækket af et barberblad og derefter efterladt i luft
Forskere opdager ny type selvhelbredende materialeØverste panel:Optiske mikroskopbilleder af beskadigede (venstre) og reparerede (højre) prøver af et af materialerne i luft ved 25 °C. En film blev knækket af et barberblad og derefter efterladt i luft
- Hvordan man laver Hummingbird Food til Feeders
- Nanoantenne koncentrerer lyset:Intensiteten øges 1, 000 gange
- Kvantehastighedsgrænser er faktisk ikke kvante
- Modificeret bakterie omdanner petroleum direkte til byggesten til plast
- Opdaget:Optimale magnetfelter til at undertrykke ustabiliteter i tokamaks
- Sådan beregnes cellekoncentration


