Grahams lov om effusion:Molær masse og gashastighed
Dette forhold er kendt som Grahams lov om effusion :
```
Rate₁ / Rate₂ =√(M₂ / M₁)
```
Hvor:
* Pris₁ er udstrømningshastigheden af gas 1
* Pris₂ er udstrømningshastigheden af gas 2
* M₁ er den molære masse af gas 1
* M₂ er den molære masse af gas 2
Forklaring:
Effusionshastigheden bestemmes af den gennemsnitlige hastighed af gasmolekylerne. Lettere molekyler bevæger sig hurtigere end tungere molekyler ved samme temperatur. Dette skyldes, at den kinetiske energi af et gasmolekyle er proportional med dets temperatur og dets masse.
Derfor har lettere molekyler en højere gennemsnitshastighed og strømmer dermed hurtigere ud gennem en lille åbning.
Eksempel:
Overvej helium (He) og oxygen (O₂). Helium har en molær masse på 4 g/mol, mens oxygen har en molær masse på 32 g/mol.
Ifølge Grahams lov:
```
Rate(He) / Rate(O₂) =√(32 / 4) =√8 ≈ 2,83
```
Det betyder, at helium strømmer ud omkring 2,83 gange hurtigere end ilt.
Applikationer:
Grahams lov har flere anvendelser inden for kemi og fysik, herunder:
* Atskille gasser: Gasser med forskellige molmasser kan adskilles ved at lade dem strømme ud gennem en porøs membran.
* Bestemmelse af molær masse: Molmassen af en ukendt gas kan bestemmes ved at sammenligne dens effusionshastighed med den for en kendt gas.
* Forståelse af gasdiffusion: Begrebet effusionshastighed er også relateret til diffusionen af gasser, som er bevægelsen af gasmolekyler fra et område med høj koncentration til et område med lav koncentration.
Sidste artikelForståelse af 'l' i kemi:kvantetal og mere
Næste artikelKaliumflammetest:Forståelse af farveemission af K₂O og KCl
 Varme artikler
Varme artikler
-
 Kædelængde bestemmer molekylær farve, muliggør farvejustering til medicinsk billeddannelseDisse polymerer, set her under UV -lys, er sammensat af nøjagtig de samme komponenter. Den eneste forskel er deres kædelængde. Kredit:Suiying Ye / ETH Zürich Jorden rundt, der udføres i øjeblikket
Kædelængde bestemmer molekylær farve, muliggør farvejustering til medicinsk billeddannelseDisse polymerer, set her under UV -lys, er sammensat af nøjagtig de samme komponenter. Den eneste forskel er deres kædelængde. Kredit:Suiying Ye / ETH Zürich Jorden rundt, der udføres i øjeblikket -
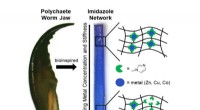 Forskere efterligner en ormedødelig kæbe for at designe og danne elastiske materialerForskere skabte en bioinspireret gradient i mekaniske egenskaber. Området opnås ved at programmere tætheden af en speciel interaktion mellem metalioner og elektrondonerende ligander. Det venstre bil
Forskere efterligner en ormedødelig kæbe for at designe og danne elastiske materialerForskere skabte en bioinspireret gradient i mekaniske egenskaber. Området opnås ved at programmere tætheden af en speciel interaktion mellem metalioner og elektrondonerende ligander. Det venstre bil -
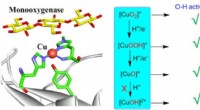 Teoretisk perspektiv på C-H/O-H-aktivering af Cu-O i biologiske og syntetiske systemerDioxygenaktivering med mononukleært kobber i biologiske og syntetiske systemer kan generere forskellige kobber-oxygen-mellemprodukter, herunder [CuO2 ]+ , [CuOOH]+ , [CuO]+ , [CuOH]2+ . Alle disse art
Teoretisk perspektiv på C-H/O-H-aktivering af Cu-O i biologiske og syntetiske systemerDioxygenaktivering med mononukleært kobber i biologiske og syntetiske systemer kan generere forskellige kobber-oxygen-mellemprodukter, herunder [CuO2 ]+ , [CuOOH]+ , [CuO]+ , [CuOH]2+ . Alle disse art -
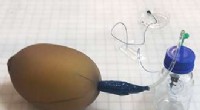 DIY-pumpe tager videnskaben ud af laboratorietForskere har udviklet en billig og enkel pumpe, lavet af balloner og strømper, som kan bruges til at analysere vand- og blodprøver uden for laboratoriet. Kredit:Walter og Eliza Hall Institute of Medic
DIY-pumpe tager videnskaben ud af laboratorietForskere har udviklet en billig og enkel pumpe, lavet af balloner og strømper, som kan bruges til at analysere vand- og blodprøver uden for laboratoriet. Kredit:Walter og Eliza Hall Institute of Medic
- En proces, der reducerer mængden af skader, som minedrift gør for økosystemer, er?
- Sådan løses lineær programmering i Excel
- Kodeskift:Presset på folk for at ændre måden, de taler på
- Hvordan fungerer mikroprocessorer inde i vækkeure?
- Hvilken astronom beskrev Jorden som universets centrum?
- Hvilke energiressourcer findes over jordoverfladen?


