Vandets kemi:Forståelse af H₂O-formlen
* Oxygens behov: Ilt har 6 elektroner i sin ydre skal og skal bruge 2 mere for at opnå en stabil oktet.
* Brintens behov: Hydrogen har 1 elektron i sin ydre skal og har brug for 1 mere for at opnå en stabil konfiguration.
Klæbningen:
* Et oxygenatom deler sine elektroner med to brintatomer og danner to kovalente bindinger.
* Hvert brintatom deler sin enkelte elektron med ilten og fuldender sin egen ydre skal.
* Denne deling resulterer i et stabilt molekyle, hvor oxygenatomet har en fuld ydre skal med 8 elektroner, og hvert brintatom har en fuld ydre skal med 2 elektroner.
Hvorfor ikke andre kombinationer?
* H2O2 (hydrogenperoxid): Mens det også indeholder brint og oxygen, er bindingen anderledes. Det har to oxygenatomer bundet til hinanden, og hvert oxygenatom har en enkeltbinding med et hydrogenatom. Dette resulterer i et helt andet molekyle med forskellige egenskaber.
* Andre kombinationer: Andre kombinationer, som H₃O eller HO, ville ikke være stabile, fordi de ikke opfylder oktetreglen for de involverede atomer. Ilt skal have 8 elektroner, og brint skal have 2 for at opnå stabilitet.
Som konklusion repræsenterer formlen H2O den specifikke måde, hvorpå hydrogen- og oxygenatomer binder sig for at skabe et stabilt vandmolekyle. Denne formel er altid konsistent, fordi de kemiske egenskaber af brint og oxygen dikterer det specifikke forhold mellem atomer, der er nødvendige for en stabil binding.
 Varme artikler
Varme artikler
-
 Legeringer fra laserprinterenDisse små prøver er lavet af oxiddispersion-forstærkede titaniumaluminider og er blevet lavet som en del af ph.d.-arbejdet. Kredit:Empa I fremtiden, nye designerlegeringer til rumfartsapplikatione
Legeringer fra laserprinterenDisse små prøver er lavet af oxiddispersion-forstærkede titaniumaluminider og er blevet lavet som en del af ph.d.-arbejdet. Kredit:Empa I fremtiden, nye designerlegeringer til rumfartsapplikatione -
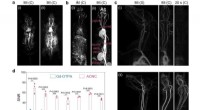 En simpel opskrift på MR-kontraster er op til fire gange højereIn vivo MR angiografi. a, b Kontrastforstærket MR-angiografi (MRA) billeder af hele kroppen på en rotte og b kanin umiddelbart efter bolusinjektionen af (i) Gd-DTPA og (ii) ACNC. c MRA-billeder af o
En simpel opskrift på MR-kontraster er op til fire gange højereIn vivo MR angiografi. a, b Kontrastforstærket MR-angiografi (MRA) billeder af hele kroppen på en rotte og b kanin umiddelbart efter bolusinjektionen af (i) Gd-DTPA og (ii) ACNC. c MRA-billeder af o -
 En farverig detektorKredit:Pixabay/CC0 Public Domain Forskere ved University of Tsukuba har udviklet en ny slags farveskiftende krystallinsk materiale, der kan bruges til at indikere tilstedeværelsen af vand. Ændri
En farverig detektorKredit:Pixabay/CC0 Public Domain Forskere ved University of Tsukuba har udviklet en ny slags farveskiftende krystallinsk materiale, der kan bruges til at indikere tilstedeværelsen af vand. Ændri -
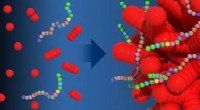 Koralformede nanopartikler bygget af design ved hjælp af konstruerede peptoiderI en ny undersøgelse ledet af PNNL-materialeforsker Chun-Long Chen, sekvensdefinerede peptoider (vist her som kæder af små farverige kugler) muliggjorde den forudsigelige morfologiske udvikling af sfæ
Koralformede nanopartikler bygget af design ved hjælp af konstruerede peptoiderI en ny undersøgelse ledet af PNNL-materialeforsker Chun-Long Chen, sekvensdefinerede peptoider (vist her som kæder af små farverige kugler) muliggjorde den forudsigelige morfologiske udvikling af sfæ
- Nye effektive skibe vil ikke være nok til at dæmpe skibssektorens miljøskader
- Hvilken temperaturskala dobbeltes den gennemsnitlige kinetiske energi af molekyler, når det er dobb…
- Ny MD-simulering kaster lys over mysteriet med hydratiserede elektroners struktur
- Saltfarver og glans:Beyond White og Metallic
- Hvad er farven på stjerner, der er mindst varm?
- Dine Facebook-venner mener det ikke, men de skader dig sandsynligvis dagligt:studie


