Sølvnitrat- og natriumchloridreaktion:Produkter og forklaring
* Sølvchlorid (AgCl) , et hvidt bundfald, der er uopløseligt i vand.
* Natriumnitrat (NaNO₃) , som forbliver opløst i opløsningen.
Den afbalancerede kemiske ligning for denne reaktion er:
AgNO₃(aq) + NaCl(aq) → AgCl(s) + NaNO₃(aq)
Her er en oversigt over reaktionen:
* Sølvionerne (Ag⁺) fra sølvnitrat reagerer med chloridionerne (Cl⁻) fra natriumchlorid.
* Disse ioner kombineres og danner sølvchlorid (AgCl), som er uopløseligt i vand og derfor udfælder ud af opløsningen som et hvidt fast stof.
* De resterende natriumioner (Na⁺) og nitrationer (NO₃⁻) forbliver opløst i opløsningen som natriumnitrat (NaNO₃).
Denne reaktion bruges ofte i kemidemonstrationer for at illustrere dobbeltforskydningsreaktioner og dannelsen af bundfald.
 Varme artikler
Varme artikler
-
 Ramanome-databasen kan hjælpe med at udvinde mikroalgecellefabrikker for at reducere kulstofemissio…Maskinindlæring af ramanomer hjælper med at screene mikroalgalcellefabrikker, der reparerer kuldioxid. Kredit:LIU Yang Mikroalger er simple organismer af enkeltceller, Alligevel giver de et stort
Ramanome-databasen kan hjælpe med at udvinde mikroalgecellefabrikker for at reducere kulstofemissio…Maskinindlæring af ramanomer hjælper med at screene mikroalgalcellefabrikker, der reparerer kuldioxid. Kredit:LIU Yang Mikroalger er simple organismer af enkeltceller, Alligevel giver de et stort -
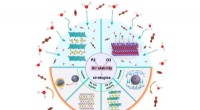 Luftstabilitet af natriumbaserede lagdelte oxidkatodematerialerAdskillige mekanismer og strategier blev vist i denne graf vedrørende luftfølsomheden af lagdelte natriumkatodematerialer. Kredit:Science China Press Natrium-ion-batterier anses for at være et af
Luftstabilitet af natriumbaserede lagdelte oxidkatodematerialerAdskillige mekanismer og strategier blev vist i denne graf vedrørende luftfølsomheden af lagdelte natriumkatodematerialer. Kredit:Science China Press Natrium-ion-batterier anses for at være et af -
 Verdensnyhed:Ny polymer går en tur, når den er oplystTimelapse-billede af gåapparatet. Kredit:Bart van Overbeeke. Forskere ved Eindhoven University of Technology og Kent State University har udviklet et nyt materiale, der kan bølge og derfor drive s
Verdensnyhed:Ny polymer går en tur, når den er oplystTimelapse-billede af gåapparatet. Kredit:Bart van Overbeeke. Forskere ved Eindhoven University of Technology og Kent State University har udviklet et nyt materiale, der kan bølge og derfor drive s -
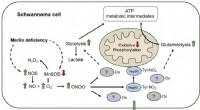 Forskere tager et vigtigt skridt mod kræftbehandlinger, der efterlader sunde celler uskadteForskere har åbnet en mulig vej til nye kræftbehandlinger, der ikke har de bivirkninger, der ofte ledsager mange nuværende kræftbehandlinger ved at identificere en proteinmodifikation, der specifikt u
Forskere tager et vigtigt skridt mod kræftbehandlinger, der efterlader sunde celler uskadteForskere har åbnet en mulig vej til nye kræftbehandlinger, der ikke har de bivirkninger, der ofte ledsager mange nuværende kræftbehandlinger ved at identificere en proteinmodifikation, der specifikt u
- Hvis månen reflekterer sollys, hvordan ser du Moon?
- En anvendelse af at bruge DNA-teknologi til at hjælpe miljøforskere ville være?
- Ny lysende kvasar opdaget af astronomer
- Hvad er meningen med ligning?
- Hvordan kan forskere redegøre for de millioner af proteiner, der er?
- Hvad beskriver bedst ordhypotesen?


