Kemiske koefficienter:Forståelse af støkiometri i kemi
Her er en oversigt:
* Hvad fortæller det os? Koefficienter fortæller os støkiometrien af en reaktion. Det betyder, at de viser de nøjagtige proportioner af involverede reaktanter og produkter.
* Ikke om atomer: Koefficienter ikke fortæl os antallet af atomer i et molekyle. Det er, hvad abonnementer gør.
* Balanceringsligninger: Koefficienter er afgørende for at afbalancere kemiske ligninger, hvilket sikrer, at antallet af atomer i hvert element er det samme på begge sider af ligningen.
Eksempel:
Overvej den balancerede ligning for forbrænding af metan:
```
CH4 + 2O2 → CO2 + 2H2O
```
* Koefficient på 1: Foran CH4 (metan)
* Koefficient på 2: Foran O2 (ilt)
* Koefficient på 1: Foran CO2 (kuldioxid)
* Koefficient på 2: Foran H2O (vand)
Dette betyder:
* 1 muldvarp af metan reagerer med 2 mol ilt til at producere 1 mol kuldioxid og 2 mol af vand.
Nøglepunkter
* Koefficienter er altid hele tal.
* En koefficient på "1" udelades normalt.
* Koefficienter kan ændres til balanceligninger, men subscripts kan ikke ændres.
Forståelse af koefficienter er afgørende for nøjagtigt at fortolke og manipulere kemiske reaktioner. De giver os mulighed for at forudsige mængden af involverede reaktanter og produkter, hvilket er afgørende for mange anvendelser inden for kemi og videre.
 Varme artikler
Varme artikler
-
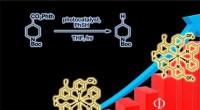 Inspireret af fotosyntese, forskere dobbeltreaktion kvanteeffektivitetReaktionens kvanteudbytte, sådan måler forskere effektiviteten af en lysaktiveret reaktion. Kredit:Anna Zieleniewska. Ud fra inspiration fra fotosyntese og den måde, hvorpå den kan opnå høj effe
Inspireret af fotosyntese, forskere dobbeltreaktion kvanteeffektivitetReaktionens kvanteudbytte, sådan måler forskere effektiviteten af en lysaktiveret reaktion. Kredit:Anna Zieleniewska. Ud fra inspiration fra fotosyntese og den måde, hvorpå den kan opnå høj effe -
 Omdanne affald til biobaserede kemikalierKredit:Pixabay/CC0 Public Domain Forskere ved Berkeley Lab har transformeret lignin, et affaldsprodukt fra papirindustrien, til en forløber for et nyttigt kemikalie med en bred vifte af potentiell
Omdanne affald til biobaserede kemikalierKredit:Pixabay/CC0 Public Domain Forskere ved Berkeley Lab har transformeret lignin, et affaldsprodukt fra papirindustrien, til en forløber for et nyttigt kemikalie med en bred vifte af potentiell -
 Mat lokkemad, kroger og ødelægger forurenende stoffer i vandPletter af titaniumdioxid klæber til polyvinylfibre i en måtte udviklet på det Rice University-ledede NEWT Center for at opfange og ødelægge forurenende stoffer fra spildevand eller drikkevand. Efter
Mat lokkemad, kroger og ødelægger forurenende stoffer i vandPletter af titaniumdioxid klæber til polyvinylfibre i en måtte udviklet på det Rice University-ledede NEWT Center for at opfange og ødelægge forurenende stoffer fra spildevand eller drikkevand. Efter -
 Læskedrikkebiprodukter kan reducere den globale opvarmningKredit:CC0 Public Domain Professor i kemi Craig Teague og hans studerende har opdaget, at biprodukterne fra læskedrikke kan hjælpe med at reducere den globale opvarmning. Et team af forskere fra
Læskedrikkebiprodukter kan reducere den globale opvarmningKredit:CC0 Public Domain Professor i kemi Craig Teague og hans studerende har opdaget, at biprodukterne fra læskedrikke kan hjælpe med at reducere den globale opvarmning. Et team af forskere fra
- Hvad er forskellen mellem en unicellulær og multicellulær organisation?
- Hvilken farve vil blåt lakmuspapir dreje i nærvær af jern II -sulfid?
- Let kerne forudsagde at være stabil på trods af at have to mærkelige kvarker
- Hvad ved vi – og ikke ved – om fracking?
- Hvordan skaber tidevand energi?
- Vil formørkelsen forårsage skade på mine øjne?


