Bekræftelse af fuldstændig reaktion:Fjernelse af ammoniak og salpetersyrerester
Forstå reaktionen:
* Ammoniak (NH3) og salpetersyre (HNO3) reagerer og danner ammoniumnitrat (NH4NO3):
NH3 (aq) + HNO3 (aq) → NH4NO3 (aq)
Metoder til at sikre, at ingen reaktanter er tilbage:
1. Støkiometri og overskydende reaktant:
* Beregn det nøjagtige støkiometriske forhold: Dette er det ideelle forhold mellem ammoniak og salpetersyre, der er nødvendigt for fuldstændig reaktion.
* Brug et overskud af én reaktant: Ved bevidst at tilføje mere af en reaktant end nødvendigt, sikrer du, at den anden reaktant er fuldt opbrugt. Dette er en fælles strategi.
* Eksempel: Hvis du vil lave 1 mol ammoniumnitrat, skal du bruge 1 mol ammoniak og 1 mol salpetersyre. Du kan tilføje 1,1 mol ammoniak for at sikre, at al salpetersyre reagerer.
2. Titrering:
* Brug en pH-indikator: Ammoniak er basisk, og salpetersyre er sur. Ved at overvåge reaktionsblandingens pH kan du bestemme, hvornår opløsningen har nået en neutral pH, hvilket indikerer, at begge reaktanter er blevet forbrugt.
3. Kemiske tests:
* Test for ammoniak: Ammoniumsalte kan påvises ved opvarmning af reaktionsblandingen. Hvis der frigives ammoniakgas, indikerer det tilstedeværelsen af uomsat ammoniak.
* Test for salpetersyre: Salpetersyre kan testes for at bruge et lakmuspapir. Hvis lakmuspapiret bliver rødt, indikerer det tilstedeværelsen af uomsat salpetersyre.
4. Fordampning og krystallisation:
* Fordamp vandet: Ammoniumnitrat er et fast stof. Ved at fordampe vandet fra reaktionsblandingen vil eventuel resterende ammoniak eller salpetersyre også blive fordampet, hvilket kun efterlader ammoniumnitrat.
* Krystallisering: Ammoniumnitrat krystalliserer let. Hvis opløsningen køles af og krystalliseres, fjernes eventuel resterende ammoniak eller salpetersyre fra opløsningen.
Hvorfor dette betyder noget:
* Produktets renhed: Rester af reaktanter kan forurene produktet, hvilket gør det uegnet til dets tilsigtede anvendelse.
* Sikkerhed: Nogle reaktanter, såsom salpetersyre, kan være ætsende eller farlige. At sikre deres fuldstændige reaktion forhindrer potentielle farer.
* Udbytte: Ufuldstændige reaktioner resulterer i lavere udbytter, hvilket betyder, at du får mindre af det ønskede produkt.
Vigtige bemærkninger:
* Omhyggelig overvågning: Ovenstående metoder kræver omhyggelig overvågning og kan have behov for justeringer baseret på de specifikke reaktionsbetingelser.
* Sikkerhedsforanstaltninger: Håndter altid kemikalier med passende sikkerhedsforanstaltninger, såsom at bære handsker og øjenværn.
Fortæl mig, hvis du har et specifikt scenario i tankerne, så kan jeg give mere skræddersyet rådgivning.
Sidste artikelMethyl Orange Dissociation Constant (Ka):Egenskaber og betydning
Næste artikelEddikesyre:Forståelse af pH-niveauer og typer
 Varme artikler
Varme artikler
-
 Dehydrerer planteproteiner med lydens hastighedEfter 8 minutter, den tørrede gel danner flager, der er lette og ikke-klæbende. Foto af Fred Zwicky Næsten alle kender til ultralyd – de højfrekvente lydbølger, der hopper rundt i kroppen og skabe
Dehydrerer planteproteiner med lydens hastighedEfter 8 minutter, den tørrede gel danner flager, der er lette og ikke-klæbende. Foto af Fred Zwicky Næsten alle kender til ultralyd – de højfrekvente lydbølger, der hopper rundt i kroppen og skabe -
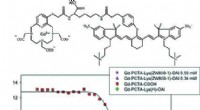 To-i-én kontrastmiddel til medicinsk billeddannelseKredit:Wiley Magnetisk resonansbilleddannelse (MRI) visualiserer indre kropsstrukturer, ofte ved hjælp af kontrastmidler for at øge følsomheden. Et belgisk hold af forskere har nu udviklet et bimo
To-i-én kontrastmiddel til medicinsk billeddannelseKredit:Wiley Magnetisk resonansbilleddannelse (MRI) visualiserer indre kropsstrukturer, ofte ved hjælp af kontrastmidler for at øge følsomheden. Et belgisk hold af forskere har nu udviklet et bimo -
 Ny produktionsteknik til højtydende polymer kunne give bedre rustningEn ny katalysator fremstillet af legerede nanopartikler af guld og palladium kan producere PBO-polymer, som bruges i kropsrustninger og andre højtydende stoffer. Den nye katalysator producerer PBO, de
Ny produktionsteknik til højtydende polymer kunne give bedre rustningEn ny katalysator fremstillet af legerede nanopartikler af guld og palladium kan producere PBO-polymer, som bruges i kropsrustninger og andre højtydende stoffer. Den nye katalysator producerer PBO, de -
 Nyopdaget kobber- og grafitkombination kan føre til mere effektive lithium-ion-batterierEn første af sin slags kobber- og grafitkombination, der blev opdaget i grundlæggende energiforskning ved det amerikanske energiministeriums Ames Laboratory, kunne have konsekvenser for at forbedre en
Nyopdaget kobber- og grafitkombination kan føre til mere effektive lithium-ion-batterierEn første af sin slags kobber- og grafitkombination, der blev opdaget i grundlæggende energiforskning ved det amerikanske energiministeriums Ames Laboratory, kunne have konsekvenser for at forbedre en
- Pennsylvania korrelerer fracking af naturgas med jordskælv
- Hvor mange kilo i 10 pund?
- Hvilken slags klippe dannes ved forvitring og erosion?
- Hvad er resterne af engang levende organismer, der findes i sedimentær klippe?
- Hvorfor er Jupiter i midten af sine universitet?
- Ny modellering viser, at intensiteten af CO₂-optagelse er højere i kystnære hav end i det åbne …


