Ideel gaslov:Forståelse af tryk, volumen, temperatur og mol
PV =nRT
hvor:
* R er den ideelle gaskonstant, som har en værdi på 8,314 J/mol·K.
Her er, hvad den ideelle gaslov fortæller os:
* Direkte proportionalitet: Trykket af en ideel gas er direkte proportional med antallet af mol og temperatur, og omvendt proportional med volumenet.
* Forudsigelseskraft: Den ideelle gaslov giver os mulighed for at forudsige opførselen af en ideel gas under forskellige forhold. For eksempel, hvis vi kender volumenet, temperaturen og antallet af mol af en gas, kan vi beregne dens tryk.
Vigtige punkter at huske om den ideelle gaslov:
* Det er en idealiseret model, hvilket betyder, at den antager, at gasmolekyler ikke har noget volumen og ikke interagerer med hinanden. Dette er ikke helt rigtigt i virkeligheden, men den ideelle gaslov er en god tilnærmelse for mange gasser ved lave tryk og høje temperaturer.
* Det gælder kun for gasser, der opfører sig ideelt. Ægte gasser kan afvige fra ideel adfærd under visse forhold.
Opsummering: Den ideelle gaslov er en grundlæggende ligning i kemi og fysik, der beskriver ideelle gassers adfærd. Det er et stærkt værktøj til at forstå og forudsige gassers egenskaber.
 Varme artikler
Varme artikler
-
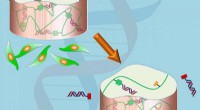 Højteknologisk gel hjælper med levering af lægemidlerGel hjælper med levering af lægemidler. Kredit:Eben Alsberg Lægemidler, der hjælper med at forhindre dannelsen af uønskede eller skadelige proteiner, er i øjeblikket ved at blive udviklet til at
Højteknologisk gel hjælper med levering af lægemidlerGel hjælper med levering af lægemidler. Kredit:Eben Alsberg Lægemidler, der hjælper med at forhindre dannelsen af uønskede eller skadelige proteiner, er i øjeblikket ved at blive udviklet til at -
 At løse et 75-årigt mysterium kan give en ny kilde til husdyrgødningTitandioxid, også kendt som titania, har fotokatalytiske egenskaber, der gør det muligt at reagere med nitrogen. Kredit:Rob Felt, Georgia Tech Løsningen på et 75-årigt materialmysterium kan en dag
At løse et 75-årigt mysterium kan give en ny kilde til husdyrgødningTitandioxid, også kendt som titania, har fotokatalytiske egenskaber, der gør det muligt at reagere med nitrogen. Kredit:Rob Felt, Georgia Tech Løsningen på et 75-årigt materialmysterium kan en dag -
 Lithium-ion-batterier får mere effektivitet på grund af silicium, germanium, kulstof nanovæggeMikrofotografi set fra siden af en elektrode skive, skildrer strukturen af en nanowall/silicium/nanowall. Kredit:Victor Krivchenko Medlemmer af D. V. Skobeltsyn Institute of Nuclear Physic og
Lithium-ion-batterier får mere effektivitet på grund af silicium, germanium, kulstof nanovæggeMikrofotografi set fra siden af en elektrode skive, skildrer strukturen af en nanowall/silicium/nanowall. Kredit:Victor Krivchenko Medlemmer af D. V. Skobeltsyn Institute of Nuclear Physic og -
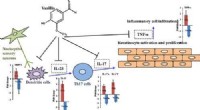 Forebyggelse af psoriasis med vanillinKredit:American Chemical Society Små mængder kunstig vaniljeekstrakt, også kendt som vanillin, findes i en bred vifte af produkter, fra bagværk til parfume. Men vanillins alsidighed stopper ikke d
Forebyggelse af psoriasis med vanillinKredit:American Chemical Society Små mængder kunstig vaniljeekstrakt, også kendt som vanillin, findes i en bred vifte af produkter, fra bagværk til parfume. Men vanillins alsidighed stopper ikke d
- Amazon tilføjer 75, 000 jobåbninger oven i de 100, 000 den allerede fyldt på en måned
- Nanofotonik teknologi muliggør en ny slags optisk spektrometer
- Ny nanoskalaparameter løser dilemmaer om siliciumegenskaber
- Ildelugtende skind giver fiskemode i Kenya
- Hvad er forskellen mellem skabelse og udvikling?
- Hvilke former ved midthavsområder?


