Magnesium- og saltsyrereaktion:En forklaring på partikelniveau
1. Opsætningen:
* Magnesium (Mg): Magnesium er et metal med en metallisk struktur. Dens atomer holdes sammen i et gitter.
* Saltsyre (HCl): Dette er en syre, og i opløsning eksisterer den som separate hydrogenioner (H+) og chloridioner (Cl-) omgivet af vandmolekyler.
2. Reaktionen:
* Kollision: Magnesiumatomer kolliderer med hydrogenioner (H+) i opløsningen.
* Elektronoverførsel: Magnesiumatomet mister to elektroner og bliver til en magnesiumion (Mg²⁺). Hydrogenionerne får hver en elektron og bliver til hydrogenatomer (H).
* Danning af hydrogengas: To brintatomer bindes til et brintmolekyle (H2), som er en gas.
* Danning af magnesiumchlorid: Magnesiumionen (Mg²⁺) kombineres med to chloridioner (Cl-) og danner magnesiumchlorid (MgCl₂), som opløses i opløsningen.
3. Den overordnede reaktion:
Den overordnede kemiske reaktion kan repræsenteres som:
Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g)
4. Observationer:
* Bobler: Du vil se bobler af brintgas dannes og stige til overfladen.
* Opløser: Magnesiummetallet vil gradvist forsvinde, efterhånden som det reagerer og danner magnesiumchlorid.
* Varme: Reaktionen frigiver varme (den er eksoterm), så opløsningen vil varme op.
Opsummering:
Reaktionen mellem magnesium og saltsyre er et klassisk eksempel på en enkelt fortrængningsreaktion. Det involverer overførsel af elektroner, hvilket resulterer i dannelsen af nye stoffer:brintgas og magnesiumchlorid.
 Varme artikler
Varme artikler
-
 Undersøgelse afslører korrosionsmekanisme af magnesiumlegeringer i marine atmosfærisk miljøDe optiske fotografier af mikrostruktur for Mg-5Y-1.5Nd-xZn-0.5Zr (x = 0, 2, 4, 6 wt.%) legeringer. Kredit:Journal of Magnesium and Alloys (2022). DOI:10.1016/j.jma.2022.03.007 Magnesiumlegeringer
Undersøgelse afslører korrosionsmekanisme af magnesiumlegeringer i marine atmosfærisk miljøDe optiske fotografier af mikrostruktur for Mg-5Y-1.5Nd-xZn-0.5Zr (x = 0, 2, 4, 6 wt.%) legeringer. Kredit:Journal of Magnesium and Alloys (2022). DOI:10.1016/j.jma.2022.03.007 Magnesiumlegeringer -
 Mikrobrygning går mere mikro(L-R) Ed Kerr og Dr. Ben Schulz har krympet kritiske øleksperimenter, potentielt fører til nye ølsorter. Kredit:Ho Vu En ph.d. studerende og ølforsker har uforvarende opdaget en måde at udføre eks
Mikrobrygning går mere mikro(L-R) Ed Kerr og Dr. Ben Schulz har krympet kritiske øleksperimenter, potentielt fører til nye ølsorter. Kredit:Ho Vu En ph.d. studerende og ølforsker har uforvarende opdaget en måde at udføre eks -
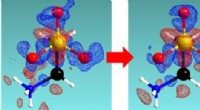 Statistisk inferens for at efterligne den meget erfarne krystallografs driftsmådePræcision af krystallografisk observation blev forbedret fra venstre mod højre ved hjælp af måledesign baseret på den foreslåede metode. Forskelle fra faktiske til sfæriske elektrontætheder er beskrev
Statistisk inferens for at efterligne den meget erfarne krystallografs driftsmådePræcision af krystallografisk observation blev forbedret fra venstre mod højre ved hjælp af måledesign baseret på den foreslåede metode. Forskelle fra faktiske til sfæriske elektrontætheder er beskrev -
 Kunstigt producerede celler kommunikerer med hinandenFørste forfatter Aurore Dupin og prof. Friedrich Simmel ved fluorescensmikroskopet. De bruger mikromanipulatorer til at samle deres kunstige cellesystemer. Kredit:Uli Benz / TUM Friedrich Simmel o
Kunstigt producerede celler kommunikerer med hinandenFørste forfatter Aurore Dupin og prof. Friedrich Simmel ved fluorescensmikroskopet. De bruger mikromanipulatorer til at samle deres kunstige cellesystemer. Kredit:Uli Benz / TUM Friedrich Simmel o


