Forståelse af kemisk reaktivitet:Faktorer, der påvirker atominteraktioner
1. Elektronkonfiguration:
* Valenselektroner: De yderste elektroner i et atom kaldes valenselektroner. Disse elektroner er involveret i kemisk binding. Atomer har en tendens til at reagere for at opnå en stabil elektronkonfiguration, normalt en fuld ydre skal (oktetregel).
* Elektronegativitet: Dette er et mål for et atoms evne til at tiltrække elektroner i en binding. Atomer med høj elektronegativitet har tendens til at få elektroner, mens atomer med lav elektronegativitet har tendens til at miste elektroner.
2. Nuklear ladning:
* Antal protoner: Antallet af protoner i kernen bestemmer atomnummeret og styrken af den positive ladning. Højere nuklear ladning tiltrækker elektroner stærkere.
3. Energiniveauer og orbitaler:
* Energiniveauer: Elektroner optager specifikke energiniveauer i et atom. Atomer reagerer for at opnå en lavere energitilstand.
* Orbitaler: Elektroner optager specifikke orbitaler inden for energiniveauer. Formen og orienteringen af orbitaler påvirker bindingen.
4. Ioniseringsenergi og elektronaffinitet:
* Ioniseringsenergi: Den energi, der kræves for at fjerne en elektron fra et atom. Atomer med lav ioniseringsenergi har en tendens til at miste elektroner.
* Elektronaffinitet: Energien ændres, når en elektron føjes til et neutralt atom. Atomer med høj elektronaffinitet har tendens til at få elektroner.
5. Typer af kemiske bindinger:
* ioniske bindinger: Dannet ved overførsel af elektroner mellem atomer, hvilket skaber ioner med modsatte ladninger. Disse bindinger forekommer normalt mellem atomer med væsentligt forskellig elektronegativitet.
* Kovalente bindinger: Dannet ved deling af elektroner mellem atomer. Disse bindinger forekommer normalt mellem atomer med lignende elektronegativitet.
* Metallige bindinger: Opstår mellem metalatomer, hvor elektroner er delokaliseret gennem metalgitteret.
6. Andre faktorer:
* Temperatur: Øget temperatur øger ofte hastigheden af kemiske reaktioner.
* Tryk: For reaktioner, der involverer gasser, kan øget tryk favorisere reaktioner, der producerer færre gasmolekyler.
* Tilstedeværelse af katalysatorer: Katalysatorer fremskynder kemiske reaktioner uden at blive forbrugt i processen.
Sammenfattende afhænger et atoms tendens til at reagere af dets elektronkonfiguration, kerneladning, energiniveauer og potentialet for at danne stabile bindinger med andre atomer. Disse faktorer bestemmer, hvor let et atom kan vinde, miste eller dele elektroner for at nå en mere stabil tilstand.
 Varme artikler
Varme artikler
-
 Forskere skal undersøge, om metalkorroderende mikrober kan vokse i Canadas foreslåede atomaffaldsa…Kredit:Pixabay/CC0 Public Domain Med Canada tættere på at flytte alt sit brugte nukleare brændsel til en enkelt facilitet og indkapsle hver brændstofbeholder i bentonit-ler, studerer forskere, om d
Forskere skal undersøge, om metalkorroderende mikrober kan vokse i Canadas foreslåede atomaffaldsa…Kredit:Pixabay/CC0 Public Domain Med Canada tættere på at flytte alt sit brugte nukleare brændsel til en enkelt facilitet og indkapsle hver brændstofbeholder i bentonit-ler, studerer forskere, om d -
 Sådan tilberedes en 5 % saltvandsopløsning:Trin-for-trin-vejledningAf Claire Gillespie | Opdateret 24. marts 2022 Sebalos/iStock/GettyImages En saltvandsopløsning er simpelthen en blanding af natriumchlorid (salt) og vand. I en vægtprocent (w/v) opløsning er saltet
Sådan tilberedes en 5 % saltvandsopløsning:Trin-for-trin-vejledningAf Claire Gillespie | Opdateret 24. marts 2022 Sebalos/iStock/GettyImages En saltvandsopløsning er simpelthen en blanding af natriumchlorid (salt) og vand. I en vægtprocent (w/v) opløsning er saltet -
 Krystaller, der renser naturgasNår de er fjernet for forurenende stoffer, naturgas brænder meget mere rent end andre fossile brændstoffer. Kredit:© Yevhen Tarnavskyi/ Shutterstock, Inc. Fjernelse af de besværlige urenheder af s
Krystaller, der renser naturgasNår de er fjernet for forurenende stoffer, naturgas brænder meget mere rent end andre fossile brændstoffer. Kredit:© Yevhen Tarnavskyi/ Shutterstock, Inc. Fjernelse af de besværlige urenheder af s -
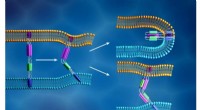 Neutroner sonderer biologiske materialer for at få indsigt i COVID-19-virusinfektionDen nye coronavirus-membran (lyseblå) og den humane cellemembran (orange) smelter sammen, når den virale S2-underenheds fusionspeptid (lilla pile) indsættes i cellemembranen, og en anden komponent af
Neutroner sonderer biologiske materialer for at få indsigt i COVID-19-virusinfektionDen nye coronavirus-membran (lyseblå) og den humane cellemembran (orange) smelter sammen, når den virale S2-underenheds fusionspeptid (lilla pile) indsættes i cellemembranen, og en anden komponent af
- Hvad er Cell City -analogien til lysosom?
- Giftige edderkopper i Northeast
- Indisk hovedstad lancerer kampagne for at begrænse giftig luftforurening
- Undersøgelse giver et detaljeret kig på spændende egenskaber ved kirale materialer
- Er brint et sjældent grundstof i universet som helhed?
- Hvordan transporteres syrer?


