Reaktioner, der involverer frie elementer:Hvad kan ikke reagere?
1. Nedbrydningsreaktioner:
* Definition: En enkelt forbindelse nedbrydes til to eller flere simplere stoffer.
* Eksempel: CaCO₃ (calciumcarbonat) → CaO (calciumoxid) + CO₂ (kuldioxid)
* Hvorfor er gratis elementer usandsynlige: Nedbrydningsreaktioner involverer nedbrydning af en forbindelse, ikke dannelse af den fra enklere grundstoffer.
2. Dobbeltforskydningsreaktioner (metatese):
* Definition: To reaktanter udveksler ioner, hvilket fører til dannelsen af to nye forbindelser.
* Eksempel: AgNO₃ (sølvnitrat) + NaCl (natriumchlorid) → AgCl (sølvchlorid) + NaNO₃ (natriumnitrat)
* Hvorfor er gratis elementer usandsynlige: Disse reaktioner involverer udskiftning af ioner inden for eksisterende forbindelser.
3. Forbrændingsreaktioner (specifik type):
* Definition: En hurtig reaktion, der involverer et stof med en oxidant (normalt oxygen), der producerer varme og lys.
* Eksempel: CH4 (methan) + 2O₂ (ilt) → CO₂ (kuldioxid) + 2H₂O (vand)
* Hvorfor er gratis elementer usandsynlige: Mens nogle forbrændingsreaktioner involverer frie elementer (som eksemplet ovenfor), involverer mange forbindelser som kulhydrater, brændstoffer eller andre organiske molekyler.
Vigtige bemærkninger:
* Undtagelser: Der er nogle reaktioner, hvor et frit grundstof kan være et produkt af en nedbrydningsreaktion. For eksempel nedbrydningen af hydrogenperoxid (H2O2) til vand (H2O) og oxygen (O2).
* Kontekst betyder noget: Hvorvidt et frit grundstof er involveret afhænger i høj grad af de specifikke reaktionsbetingelser. For eksempel kan en reaktion involvere et frit grundstof som en katalysator eller en reaktant i et meget specifikt miljø.
Nøgleudtag:
Mens mange reaktioner kan involvere frie elementer som reaktanter (som kombinationsreaktioner), gør nedbrydning, dobbelt forskydning og visse typer forbrændingsreaktioner det normalt ikke.
Sidste artikelBrintproduktion fra vand:En omfattende vejledning
Næste artikelOxygendibromid (OBr₂):Kovalent karakter forklaret
 Varme artikler
Varme artikler
-
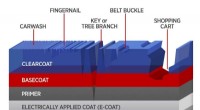 For at forbedre auto -belægninger, nye tests gør mere end at ridse overfladenSkematisk af belægningslagene i et typisk bilkomposithus. Mar- og ridseskader fra forskellige objektpåvirkninger vises. Kredit:Eastman Chemical Co./ K. Irvine, NIST Kender du den kvalmende følelse
For at forbedre auto -belægninger, nye tests gør mere end at ridse overfladenSkematisk af belægningslagene i et typisk bilkomposithus. Mar- og ridseskader fra forskellige objektpåvirkninger vises. Kredit:Eastman Chemical Co./ K. Irvine, NIST Kender du den kvalmende følelse -
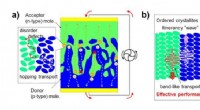 Sporing af ladningsbærere i den molekylære krystal ved organisk pn-forbindelse(a) Hoppeledning i uordnet kryds, (b) båndledning i krystallinsk forbindelse. Kredit:NINS/IMS I konventionelle organiske solceller, elektronerne udviser deres partikel-natur og skal hoppe mellem o
Sporing af ladningsbærere i den molekylære krystal ved organisk pn-forbindelse(a) Hoppeledning i uordnet kryds, (b) båndledning i krystallinsk forbindelse. Kredit:NINS/IMS I konventionelle organiske solceller, elektronerne udviser deres partikel-natur og skal hoppe mellem o -
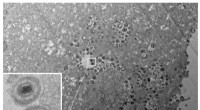 Ekstrem kulde kan afsløre herpesvirus infektionsdynamikEt transmissionselektronmikroskopbillede viser varicella-zoster-virussen. En avanceret version, kryogen elektronmikroskopi, kunne afsløre endnu flere detaljer, herunder hvordan virus inficerer celler.
Ekstrem kulde kan afsløre herpesvirus infektionsdynamikEt transmissionselektronmikroskopbillede viser varicella-zoster-virussen. En avanceret version, kryogen elektronmikroskopi, kunne afsløre endnu flere detaljer, herunder hvordan virus inficerer celler. -
 Hvorfor bliver dit bomuldshåndklæde stift efter naturlig tørring?Et bomuldsbundt efter naturlig tørring blev stift, som om det var limet (til venstre), hvorimod den, der blev tørret ved tvungen dræning i en vaskemaskine sammen med fysisk omrøring, såsom rystning, f
Hvorfor bliver dit bomuldshåndklæde stift efter naturlig tørring?Et bomuldsbundt efter naturlig tørring blev stift, som om det var limet (til venstre), hvorimod den, der blev tørret ved tvungen dræning i en vaskemaskine sammen med fysisk omrøring, såsom rystning, f
- Isotopiske beviser afslører overraskende kostvaner hos gamle jæger-samlere
- Hvor lang tid ville det tage at nå Jupiter på vores hurtigste bemandede raket?
- Alger på floden, der løber ud i Lake Erie, giver en advarsel
- Er flydende en stubtance, der ikke kan opdeles i enklere stof?
- At blive negativ betaler for nanorør:Team finder mulige nøgler til bedre nanofibre, film
- Hvilke kontinentoverflade ligner overfladen?


