Neutraliseringsvarme:HCl og NaOH forklaret - Kemi
Her er hvorfor:
* Stærke syrer og baser dissocieres fuldstændigt i vand. Det betyder, at HCl og NaOH eksisterer som henholdsvis H+ og Cl- ioner og Na+ og OH- ioner i opløsning.
* Neutraliseringsreaktionen involverer i det væsentlige dannelsen af vand. H+-ionen fra syren reagerer med OH-ionen fra basen og danner vand (H2O):
H+ (aq) + OH- (aq) → H2O (l)
* Neutraliseringsvarmen er entalpiændringen for denne reaktion. Da stærke syrer og baser dissocierer fuldstændigt, er neutralisationsvarmen i det væsentlige entalpiændringen for dannelsen af vand fra dets ioner, hvilket er en konstant værdi.
Vigtige bemærkninger:
* Neutralisationsvarmen kan variere lidt afhængigt af de specifikke koncentrationer af den anvendte syre og base.
* Denne værdi på -57,3 kJ/mol gælder for reaktioner ved standardbetingelser (298 K og 1 atm).
Sig til, hvis du har andre spørgsmål.
 Varme artikler
Varme artikler
-
 Sikker opbevaring af rent cæsium:Sikkerhedsstandarder og bedste praksisLYagovy/iStock/GettyImages Oversigt over cæsium Cæsium er et sjældent, meget reaktivt alkalimetal, med kun omkring 55.000 pund forbrugt på verdensplan hvert år. Dens primære anvendelse er i olieborem
Sikker opbevaring af rent cæsium:Sikkerhedsstandarder og bedste praksisLYagovy/iStock/GettyImages Oversigt over cæsium Cæsium er et sjældent, meget reaktivt alkalimetal, med kun omkring 55.000 pund forbrugt på verdensplan hvert år. Dens primære anvendelse er i olieborem -
 En balancegang:Forbedret vandbehandlingsteknik ved hjælp af energitilpasningMangel på ferskvand i mange dele af verden kræver forbedrede og bæredygtige metoder til spildevandsrensning. Kredit:PS Photography på Pexels I dag, et stort antal mennesker verden over lider under
En balancegang:Forbedret vandbehandlingsteknik ved hjælp af energitilpasningMangel på ferskvand i mange dele af verden kræver forbedrede og bæredygtige metoder til spildevandsrensning. Kredit:PS Photography på Pexels I dag, et stort antal mennesker verden over lider under -
 Hvorfor McDonald's Cola smager bedre:Videnskaben bag den forfriskende smagJennifer Tepp/Shutterstock Uanset om det er parret med varme, salte pommes frites eller slukker en sommertørst, smager Cola serveret på McDonalds konsekvent overlegent. Kæden tilskriver denne konsist
Hvorfor McDonald's Cola smager bedre:Videnskaben bag den forfriskende smagJennifer Tepp/Shutterstock Uanset om det er parret med varme, salte pommes frites eller slukker en sommertørst, smager Cola serveret på McDonalds konsekvent overlegent. Kæden tilskriver denne konsist -
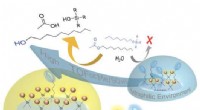 Nøglebeviser, der forbinder hydrofobicitet med effektiv syrekatalyseForenklet skematisk, der viser, hvordan alkylacetater med lange haler ikke kan nærme sig sure sulfo-steder (blå skiver) i hydrofile miljøer; imidlertid, de kan nærme sig hydrofobe miljøer med flere me
Nøglebeviser, der forbinder hydrofobicitet med effektiv syrekatalyseForenklet skematisk, der viser, hvordan alkylacetater med lange haler ikke kan nærme sig sure sulfo-steder (blå skiver) i hydrofile miljøer; imidlertid, de kan nærme sig hydrofobe miljøer med flere me
- Forskere forklarer, hvordan organiske molekyler binder sig til halvlederoverflader
- Når en organisme gengives ved spirende, hvordan begynder den nye at vokse?
- IBMs Red Hat-aftale på $34 milliarder er et risikabelt bud på at øge cloud-forretningen
- Hvorfor er bjerge konstruktive?
- Hvad er MT Shasta?
- Tencent-fortjenesten stiger, efterhånden som den dukker op fra gaming sump


