Afbalancering af kemiske ligninger:Loven om bevarelse af masse forklaret
Sådan hænger det sammen med at afbalancere kemiske ligninger:
* Atomer er omarrangeret, ikke skabt eller ødelagt: Kemiske reaktioner involverer omlejring af atomer for at danne nye molekyler. Atomerne selv forbliver uændrede.
* Balancering sikrer lige atomer på begge sider: Ved at afbalancere en kemisk ligning sikrer du, at det samme antal atomer af hvert grundstof optræder på både reaktant (udgangsmaterialer) og produkt (resulterende stoffer) sider af ligningen.
* Afspejler loven: Denne balance afspejler princippet om bevarelse af massen. Da du ikke kan skabe eller ødelægge atomer, skal den samlede masse af reaktanterne svare til den samlede masse af produkterne.
Eksempel:
Den ubalancerede ligning for forbrænding af metan er:
CH4 + O2 → CO2 + H2O
Denne ligning er ubalanceret, fordi:
* Der er 4 brintatomer til venstre, men kun 2 til højre.
* Der er 2 oxygenatomer til venstre, men 3 til højre.
For at afbalancere det tilføjer vi koefficienter:
CH₄ + 2 O₂ → CO₂ + 2 H2O
Nu har vi:
* 1 kulstofatom på begge sider
* 4 brintatomer på begge sider
* 4 iltatomer på begge sider
Denne afbalancerede ligning afspejler loven om bevarelse af masse, der sikrer, at den samlede masse af reaktanterne (methan og oxygen) er lig med den samlede masse af produkterne (kuldioxid og vand).
 Varme artikler
Varme artikler
-
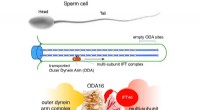 Transport af molekylære motorer til ciliaBilledet øverst viser en sædcelle med hoved (cellekrop) og hale (også kendt som flagellum eller cilium), der driver sædcellen fremad. Skemaet i midten viser, hvordan dyneinmotorer (gule stjerner) tran
Transport af molekylære motorer til ciliaBilledet øverst viser en sædcelle med hoved (cellekrop) og hale (også kendt som flagellum eller cilium), der driver sædcellen fremad. Skemaet i midten viser, hvordan dyneinmotorer (gule stjerner) tran -
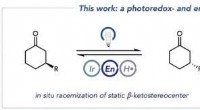 Forskere rapporterer om ny platform for stereokontrolDen overordnede transformation, der kombinerer racemisering af ketonsubstraterne (til venstre) med biokatalytisk reduktion til enantiomert rene alkoholprodukter (i midten), og den vigtigste enaminylra
Forskere rapporterer om ny platform for stereokontrolDen overordnede transformation, der kombinerer racemisering af ketonsubstraterne (til venstre) med biokatalytisk reduktion til enantiomert rene alkoholprodukter (i midten), og den vigtigste enaminylra -
 Mikrober udviklet til at omdanne sukker til et kemikalie, der findes i dæk1, 3-butadien fremstillet af bakterier. Kredit:Yokohama Rubber Dækindustriens fremtidige miljømæssige fodaftryk kan blive væsentligt formindsket takket være en ny miljøvenlig måde fundet af fire R
Mikrober udviklet til at omdanne sukker til et kemikalie, der findes i dæk1, 3-butadien fremstillet af bakterier. Kredit:Yokohama Rubber Dækindustriens fremtidige miljømæssige fodaftryk kan blive væsentligt formindsket takket være en ny miljøvenlig måde fundet af fire R -
 Første nogensinde atomopløsningsvideo af saltkrystaller, der dannes i realtidEn natriumchlorid krystal, der vokser i et vibrerende kulstof nanohorn. Kredit:© 2021 American Chemical Society To nye teknikker, atomopløsning i realtid video og konisk carbon nanorør indeslutnin
Første nogensinde atomopløsningsvideo af saltkrystaller, der dannes i realtidEn natriumchlorid krystal, der vokser i et vibrerende kulstof nanohorn. Kredit:© 2021 American Chemical Society To nye teknikker, atomopløsning i realtid video og konisk carbon nanorør indeslutnin
- Brug anden lov til at beskrive forholdet mellem kraftmasse og acceleration.?
- David og Goliat:Hvordan en lille edderkop fanger meget større bytte
- Forældre er vrede, da Delhi-skoler genåbner trods smog
- Lægemiddelleveringsplatform udnytter luftfyldte proteinnanostrukturer og bruger lyd til målretning…
- Hvad er der sket med accelerationen af et objekt, hvis du fordobler både masse og ubalanceret kra…
- Hvad er pH for jernoxid?


