Carbon Bonding:Typer og eksempler - En omfattende vejledning
* Kovalente bindinger: Disse er den mest almindelige type bindingskulstofformer. I en kovalent binding deler kulstof elektroner med et andet atom for at danne en stabil ydre skal. Denne deling kan være ens (ikke-polær) eller ulige (polær). Eksempler inkluderer bindingerne i metan (CH4), kuldioxid (CO2) og glucose (C6H12O6).
* Ionbindinger: Selvom det er mindre almindeligt, kan kulstof danne ioniske bindinger med stærkt elektronegative elementer som oxygen. I dette tilfælde mister kulstof elektroner for at danne en positivt ladet ion (kation), som derefter tiltrækkes af en negativt ladet ion (anion) af det andet grundstof. Dette ses i carbonmonoxid (CO), hvor carbon danner en delvis positiv ladning.
Her er en oversigt over de forskellige typer af kovalente bindinger carbonformer:
* Enkeltbinding: Kulstof deler en elektron med et andet atom.
* Dobbeltbinding: Kulstof deler to elektroner med et andet atom.
* Tredobbelt binding: Kulstof deler tre elektroner med et andet atom.
Nøglepunkter at huske:
* Carbons evne til at danne fire bindinger gør det muligt at skabe en lang række komplekse molekyler.
* Kulstofs evne til at danne både enkelt- og multiple bindinger bidrager til mangfoldigheden af organiske molekyler.
* Kulstofs evne til at binde sig til sig selv (catenation) er grundlaget for lange kæder og komplekse strukturer i organiske molekyler.
Sig til, hvis du vil have flere detaljer om nogen af disse punkter!
 Varme artikler
Varme artikler
-
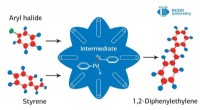 Kemiker udvikler blomsterlignende katalysatorer fra grafenKredit:RUDN University En RUDN -kemiker og kolleger fra Iran har udviklet en ny strategi til fremstilling af hule, porøse katalysatorer til Heck -koblingsreaktionen. Disse katalysatorer er kendete
Kemiker udvikler blomsterlignende katalysatorer fra grafenKredit:RUDN University En RUDN -kemiker og kolleger fra Iran har udviklet en ny strategi til fremstilling af hule, porøse katalysatorer til Heck -koblingsreaktionen. Disse katalysatorer er kendete -
 Slamdrevne bakterier genererer mere elektricitet, hurtigereKAUST-forskere har identificeret en ny elektroaktiv bakterie, kaldet Desulfuromonas acetexigens, der producerer en højere strømtæthed end en traditionelt brugt bakterie, og på kortere tid. Kredit:KAUS
Slamdrevne bakterier genererer mere elektricitet, hurtigereKAUST-forskere har identificeret en ny elektroaktiv bakterie, kaldet Desulfuromonas acetexigens, der producerer en højere strømtæthed end en traditionelt brugt bakterie, og på kortere tid. Kredit:KAUS -
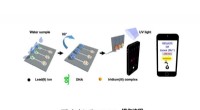 Ny enhed til hurtig og præcis detektering af blyDiagrammet viser detektionsprocessen. Kredit:HKBU Et forskerhold fra Institut for Kemi ved Hong Kong Baptist University (HKBU) har opfundet en bærbar enhed til one-stop-detektion af blykoncentrati
Ny enhed til hurtig og præcis detektering af blyDiagrammet viser detektionsprocessen. Kredit:HKBU Et forskerhold fra Institut for Kemi ved Hong Kong Baptist University (HKBU) har opfundet en bærbar enhed til one-stop-detektion af blykoncentrati -
 Forskere skaber bedre materiale til bærbare biosensorerMenneskelig hudstruktur. Kredit:Wikipedia Biosensorer, der kan bæres på menneskelig hud eller sikkert bruges inde i kroppen, er i stigende grad udbredt til både medicinske anvendelser og daglig su
Forskere skaber bedre materiale til bærbare biosensorerMenneskelig hudstruktur. Kredit:Wikipedia Biosensorer, der kan bæres på menneskelig hud eller sikkert bruges inde i kroppen, er i stigende grad udbredt til både medicinske anvendelser og daglig su
- Hvad er bevægelse af et stationært objekt?
- Hvad er sandt ved celledelingens satser i eukaryoter?
- Hvad er Jordens naturlige form for synligt lys?
- Kunne et anti-global opvarmning atmosfærisk sprøjteprogram virkelig fungere?
- Hvad er overfladetemperaturen for Alioth Star?
- Sammensatte virkninger af alvorlige vejrhændelser giver næring til marine hedebølger i kysthavet


