Elektronoverførsel i aluminium-klorbinding:en detaljeret forklaring
1. Identificer debiteringerne:
* Aluminium (Al) er i gruppe 3A, så den har 3 valenselektroner og har en tendens til at miste dem for at opnå en stabil oktet. Det danner en +3-ion (Al3+).
* Klor (Cl) er i gruppe 7A, så den har 7 valenselektroner og har en tendens til at få en elektron for at opnå en stabil oktet. Det danner en -1 ion (Cl⁻).
2. Bestem forholdet:
For at afbalancere ladningerne har vi brug for tre kloratomer (3 x -1 =-3) for at matche +3 ladningen af et aluminiumatom. Den resulterende forbindelse er aluminiumchlorid (AlCl3).
3. Tæl de overførte elektroner:
* Hvert aluminiumsatom mister 3 elektroner .
* Hvert kloratom får 1 elektron .
* Da der er tre kloratomer, i alt 3 elektroner er overført.
Derfor overføres 3 elektroner for at danne en binding mellem aluminium og klor.
Sidste artikelKemiske reaktioner:skabelse af nye stoffer forklaret
Næste artikelNitrogen vs. Arsen:Udforskning af nøgleforskelle og ligheder
 Varme artikler
Varme artikler
-
 MR -mærker klæber til molekyler med kemisk velcroI den nye teknik, MR -kemiske mærker knytter sig til et målmolekyle og intet andet - ligesom hvordan velcro kun klæber til sig selv. Kredit:tanakawho, via Flickr Forestil dig at vedhæfte et fyrtår
MR -mærker klæber til molekyler med kemisk velcroI den nye teknik, MR -kemiske mærker knytter sig til et målmolekyle og intet andet - ligesom hvordan velcro kun klæber til sig selv. Kredit:tanakawho, via Flickr Forestil dig at vedhæfte et fyrtår -
 Knækker koden for et formskiftende proteinKredit:Pixabay/CC0 Public Domain Et formskiftende immunsystemprotein kaldet XCL1 udviklede sig fra en enkelt-formede forfader for hundreder af millioner af år siden. Nu, forskere ved Medical Colle
Knækker koden for et formskiftende proteinKredit:Pixabay/CC0 Public Domain Et formskiftende immunsystemprotein kaldet XCL1 udviklede sig fra en enkelt-formede forfader for hundreder af millioner af år siden. Nu, forskere ved Medical Colle -
 Terminatorlignende flydende metal bevæger sig og strækker sig i 3D-rumKredit:American Chemical Society I blockbusteren Terminator film franchise, en ond robot forvandler sig til forskellige menneskelige former og objekter og oser gennem smalle åbninger, takket vær
Terminatorlignende flydende metal bevæger sig og strækker sig i 3D-rumKredit:American Chemical Society I blockbusteren Terminator film franchise, en ond robot forvandler sig til forskellige menneskelige former og objekter og oser gennem smalle åbninger, takket vær -
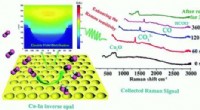 Elektroder varme kanter omdanner CO2 -gas til brændstoffer og kemikalierKredit: Journal of Materials Chemistry A (2019). DOI:10.1039/C9TA02288K Et team af forskere har skabt en skålformet elektrode med varme kanter, som effektivt kan omdanne CO 2 fra gas til kulsto
Elektroder varme kanter omdanner CO2 -gas til brændstoffer og kemikalierKredit: Journal of Materials Chemistry A (2019). DOI:10.1039/C9TA02288K Et team af forskere har skabt en skålformet elektrode med varme kanter, som effektivt kan omdanne CO 2 fra gas til kulsto
- Hvilket ville give mere energi en 1,5V celle eller 9V batteri?
- Hvad er det vigtigste kendetegn ved programmeret IO?
- Ny teknisk regulering uundgåelig, Det siger Apples administrerende direktør
- Hvorfor er vandcyklussen vigtig for et økosystem?
- Hvad er hyppigheden af en bølge med hastighed 100ms og bølgelængde 20m?
- Hvad er ny State Stone?


