Sølvopløsning i salpetersyre:kemisk reaktion og ligning
Her er den afbalancerede kemiske ligning:
3Ag(s) + 4HNO3(aq) → 3AgNO3(aq) + 2H2O(l) + 2NO2(g)
Her er en oversigt over reaktionen:
* Ag(er): Solid sølvmetal.
* HNO₃(aq): Salpetersyreopløsning.
* AgNO₃(aq): Sølvnitratopløsning.
* H2O(l): Flydende vand.
* NO₂(g): Gasformig nitrogendioxid, som er en brun-rød gas.
Forklaring:
1. Oxidation af sølv: Sølvmetal mister elektroner og bliver oxideret til sølvioner (Ag⁺).
2. Reduktion af salpetersyre: Salpetersyre fungerer som oxidationsmiddel, accepterer elektroner og reduceres til nitrogendioxid (NO₂).
3. Danning af sølvnitrat: Sølvionerne (Ag⁺) reagerer med nitrationer (NO₃⁻) fra salpetersyre og danner sølvnitrat (AgNO₃), som opløses i vand.
4. Produktion af vand: Hydrogenioner (H⁺) fra salpetersyre reagerer med hydroxidioner (OH⁻) dannet under reaktionen for at producere vand (H2O).
Nøglepunkter:
* Reaktionen er eksoterm og frigiver varme.
* Nitrogendioxidgas frigives som et biprodukt, hvilket giver en brun-rød farve.
* Sølvnitratopløsningen vil være farveløs.
Sig til, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
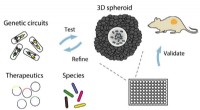 Forskere udvikler en ny platform, der genskaber kræft i et fad for hurtigt at bestemme den bedste b…Bakterier koloniserer multicellulære sfæroider in vitro, hvor de screenes for vækst, kredsløb dynamik, og terapeutisk effekt og derefter valideres i musetumormodeller. Kredit:Tetsuhiro Harimoto/Columb
Forskere udvikler en ny platform, der genskaber kræft i et fad for hurtigt at bestemme den bedste b…Bakterier koloniserer multicellulære sfæroider in vitro, hvor de screenes for vækst, kredsløb dynamik, og terapeutisk effekt og derefter valideres i musetumormodeller. Kredit:Tetsuhiro Harimoto/Columb -
 Udvikling af forenklet ny massespektrometrisk teknik ved brug af laser og grafenFormand-professor Dae Won Moon i Institut for Ny Biologi (til venstre) og forskningsstipendiat Jae Young Kim i Institut for Robotteknologi (til højre) Kredit:DGIST En teknologi, der kan opnå høj o
Udvikling af forenklet ny massespektrometrisk teknik ved brug af laser og grafenFormand-professor Dae Won Moon i Institut for Ny Biologi (til venstre) og forskningsstipendiat Jae Young Kim i Institut for Robotteknologi (til højre) Kredit:DGIST En teknologi, der kan opnå høj o -
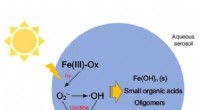 Virkninger af Fenton-lignende reaktioner af ferroloxalat på atmosfæriske oxidationsprocesser og st…Methacrolein reagerer med superoxidradikaler frembragt ved en Fenton-lignende reaktion. Dette påvirker atmosfærisk strålingsforcerende kraft på grund af dannelsen af uopløseligt jernhydroxid. Kredit
Virkninger af Fenton-lignende reaktioner af ferroloxalat på atmosfæriske oxidationsprocesser og st…Methacrolein reagerer med superoxidradikaler frembragt ved en Fenton-lignende reaktion. Dette påvirker atmosfærisk strålingsforcerende kraft på grund af dannelsen af uopløseligt jernhydroxid. Kredit -
 Kemikere bruger teknologi til at afkode sproget for lipid-protein-interaktionMembranproteinprøver infunderes i massespektrometrien ved hjælp af nanoflow elektrospray-ionisering (nESI). I dette kunstværk, frie og lipidbundne membranproteiner dukker op fra dråber i nESI-processe
Kemikere bruger teknologi til at afkode sproget for lipid-protein-interaktionMembranproteinprøver infunderes i massespektrometrien ved hjælp af nanoflow elektrospray-ionisering (nESI). I dette kunstværk, frie og lipidbundne membranproteiner dukker op fra dråber i nESI-processe
- Zebrafisk afslører, hvordan bioelektricitet former muskeludvikling
- Organiske krystaller twist, bøje, og helbrede
- Forklar, hvordan videnskabelig teori kan ændre sig?
- Hvad er det bedste college til at studere astrofysik?
- Hvad er forskellen mellem to carbonatomer med samme antal neutroner?
- Hurtigere end lydens hastighed:Nyt kontrolsystem har det, der skal til for at guide eksperimentelle …


