Fluorbinding:Kovalent vs. ionisk - Forståelse af kemiske bindinger
* Elektronegativitet: Fluor er det mest elektronegative element, hvilket betyder, at det har en stærk tiltrækning af elektroner.
* Ioniseringsenergi: Mens fluor kan få en elektron, er dens ioniseringsenergi (den energi, der kræves for at fjerne en elektron) meget høj. Det betyder, at det er svært at få det til at miste en elektron og danne en positiv ion.
* Tendens til binding: På grund af dets høje elektronegativitet og høje ioniseringsenergi foretrækker fluor at dele elektroner med andre atomer i stedet for helt at vinde eller miste dem.
Der er dog nogle undtagelser:
* Med alkalimetaller og jordalkalimetaller: Fluor kan danne ioniske bindinger med disse meget elektropositive elementer. Den store forskel i elektronegativitet fører til fuldstændig overførsel af elektroner, hvilket skaber ioner som NaF (natriumfluorid) og CaF2 (calciumfluorid).
Sammenfattende danner fluor primært kovalente bindinger på grund af dets høje elektronegativitet og vanskeligheden ved at fjerne dets elektroner. Det kan dog danne ionbindinger med stærkt elektropositive grundstoffer.
 Varme artikler
Varme artikler
-
 Fremstilling af nye materialer ved hjælp af kunstig intelligensKredit:Pohang University of Science &Technology (POSTECH) Der er et gammelt ordsprog, Hvis gummi er det materiale, der åbnede vejen til jorden, aluminium er den, der åbnede vejen til himlen. Nye m
Fremstilling af nye materialer ved hjælp af kunstig intelligensKredit:Pohang University of Science &Technology (POSTECH) Der er et gammelt ordsprog, Hvis gummi er det materiale, der åbnede vejen til jorden, aluminium er den, der åbnede vejen til himlen. Nye m -
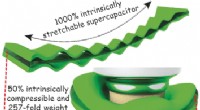 Super strækbar, superkomprimerbare superkondensatorerFleksibel, bærbar elektronik kræver lige så fleksibel, bærbare strømkilder. I journalen Angewandte Chemie , Kinesiske videnskabsmænd har introduceret en ekstraordinært strækbar og komprimerbar polye
Super strækbar, superkomprimerbare superkondensatorerFleksibel, bærbar elektronik kræver lige så fleksibel, bærbare strømkilder. I journalen Angewandte Chemie , Kinesiske videnskabsmænd har introduceret en ekstraordinært strækbar og komprimerbar polye -
 Video:Hvordan håndsprit virkerKredit:The American Chemical Society Alkoholbaserede håndsprit er de allestedsnærværende små klemflaskehelte i lufthavne og hospitaler, vores allierede i forkølelses- og influenzasæsonen, og angiv
Video:Hvordan håndsprit virkerKredit:The American Chemical Society Alkoholbaserede håndsprit er de allestedsnærværende små klemflaskehelte i lufthavne og hospitaler, vores allierede i forkølelses- og influenzasæsonen, og angiv -
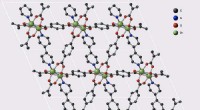 Nye materialer til opbevaring af brændbare industrigasserStruktur af metal-organisk rammeværk MOF-508, sammensat af kulstof (sort), nitrogen (blå), oxygen (rød) og zink (grøn). Fleksibiliteten og den kædede karakter af denne ramme er nøgleparametre for opbe
Nye materialer til opbevaring af brændbare industrigasserStruktur af metal-organisk rammeværk MOF-508, sammensat af kulstof (sort), nitrogen (blå), oxygen (rød) og zink (grøn). Fleksibiliteten og den kædede karakter af denne ramme er nøgleparametre for opbe
- Hvem er en rigtig mand? De fleste australiere mener, at forældede maskulinitetsidealer holder mænd…
- Det fulde spektrum af jordskælvstriggere – 3 menneskeskabte årsager
- Hvad adskiller et organisk molekyle fra og et uorganisk molekyle?
- Hvad er forskellen mellem fine og grov kornede stødende rock?
- Nyt virtual reality-værktøj giver dig mulighed for at se verden gennem øjnene på en lille primat
- Beviser for vulkanske kratere på Saturns måne Titan


