Carbonation som base:Arrhenius definition forklaret
* Arrhenius Base: En Arrhenius-base er et stof, der producerer hydroxidioner (OH-), når det opløses i vand. I den reaktion, du angav, reagerer carbonation (CO3^2-) med vand for at producere bicarbonat (HCO3-) og hydroxid (OH-).
* Brønsted-Lowry Base: En Brønsted-Lowry base er et stof, der accepterer en proton (H+). Mens carbonation ikke accepterer en proton i denne reaktion (dannende bicarbonat), er Arrhenius definition mere direkte anvendelig, fordi den specifikt fokuserer på produktionen af hydroxidioner.
Lad os nedbryde reaktionen:
CO3^2- (aq) + H2O (l) ⇌ HCO3- (aq) + OH- (aq)
* CO3^2- fungerer som en Arrhenius-base ved at acceptere en proton fra vand og producere OH-.
* H2O fungerer som en Brønsted-Lowry-syre ved at donere en proton.
Derfor fungerer carbonation-ionen som en Arrhenius-base i denne reaktion.
 Varme artikler
Varme artikler
-
 Forskere arbejder på at skabe mikrochipelementer i molekylær størrelseKredit:CC0 Public Domain Moderne siliciumbaserede integrerede kredsløb (ICer) har nået de praktiske grænser for miniaturisering, mens brugen af organiske stoffer potentielt kan tillade skabelsen
Forskere arbejder på at skabe mikrochipelementer i molekylær størrelseKredit:CC0 Public Domain Moderne siliciumbaserede integrerede kredsløb (ICer) har nået de praktiske grænser for miniaturisering, mens brugen af organiske stoffer potentielt kan tillade skabelsen -
 Kemikere skaber nyt kvasikrystalmateriale ud fra nanopartikelbyggestenFørst opdaget i 1980erne, kvasikrystaller har ordnede strukturer, der i modsætning til normale krystaller, mangler et forudsigeligt gentagelsesmønster. Kvasikrystaller har også symmetrier, der er forb
Kemikere skaber nyt kvasikrystalmateriale ud fra nanopartikelbyggestenFørst opdaget i 1980erne, kvasikrystaller har ordnede strukturer, der i modsætning til normale krystaller, mangler et forudsigeligt gentagelsesmønster. Kvasikrystaller har også symmetrier, der er forb -
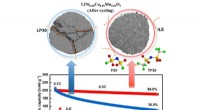 Ny kombination af materialer skaber rekordstore lithium-metalcellerDen ioniske flydende elektrolyt ILE (højre) forhindrer stort set strukturelle ændringer på den nikkelrige NCM88 katode. Efter 1000 cykler, batterikapacitet når stadig 88 procent. Kredit:Fanglin Wu og
Ny kombination af materialer skaber rekordstore lithium-metalcellerDen ioniske flydende elektrolyt ILE (højre) forhindrer stort set strukturelle ændringer på den nikkelrige NCM88 katode. Efter 1000 cykler, batterikapacitet når stadig 88 procent. Kredit:Fanglin Wu og -
 Forskere gør et vigtigt fremskridt i retning af produktion af vigtigt biobrændstofGrafisk, der viser biobutanolseparationsmetode. Kredit:Oregon State University Et internationalt forskningssamarbejde har taget et vigtigt skridt i retning af den kommercielt levedygtige fremstill
Forskere gør et vigtigt fremskridt i retning af produktion af vigtigt biobrændstofGrafisk, der viser biobutanolseparationsmetode. Kredit:Oregon State University Et internationalt forskningssamarbejde har taget et vigtigt skridt i retning af den kommercielt levedygtige fremstill
- reaktionsserier forudsiger størrelsen af forskellige mineralkorn, der vokser fra krystalliserende…
- Hvad er energioverførslen til en lampe, du tilslutter til væggen?
- Sydkorea vil søge kulstofneutralitet inden 2050:Månen
- Hvilke former, når vanddamp skifter direkte til is uden at blive en væske først?
- Hvilken planet i dit solsystem har ingen atmosfære?
- Hvad hedder alt, hvad der findes, herunder alt stof og energi


