Ioniske forbindelser:Hvorfor er de ikke altid opladet?
1. Opladningsneutralitet:
* Ioniske forbindelser dannes af den elektrostatiske tiltrækning mellem positivt ladede ioner (kationer) og negativt ladede ioner (anioner).
* Nøglen er, at disse gebyrer balancerer hinanden . Antallet af positive ladninger er nøjagtigt lig med antallet af negative ladninger, hvilket resulterer i en samlet neutral forbindelse.
2. Eksempel:
* Tag bordsalt (NaCl). Natrium (Na) mister en elektron for at blive Na+ (kation), mens klor (Cl) får en elektron til at blive Cl- (anion).
* Ladningerne balancerer perfekt:en +1 ladning fra Na+ og en -1 ladning fra Cl-.
3. Formelenheder:
* Ioniske forbindelser er ikke repræsenteret af individuelle molekyler som kovalente forbindelser. De eksisterer som gentagne, tredimensionelle strukturer kaldet formelenheder . Disse formelenheder opretholder altid ladningsbalancen.
4. Elektrolytter:
* Mens de generelt er neutrale, kan ioniske forbindelser blive ladet, når de opløses i vand. Dette skyldes, at vandmolekylerne kan adskille ionerne, hvilket fører til en opløsning, der leder elektricitet (en elektrolyt).
Opsummering: Ioniske forbindelser opnår neutralitet, fordi de er dannet af en præcis balance mellem positive og negative ladninger. Denne balance opretholdes i formlenhederne, der udgør forbindelsen.
 Varme artikler
Varme artikler
-
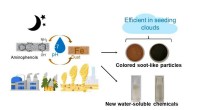 Ny kemi opstår, når støv møder forureningRepræsentation af forureningshændelser, hvor mineralstøv og biomassebrændende røg blandes. Kredit:Hind Al-Abadleh Det er en ny kemi fundet at finde sted i en skydråbe, en våd aerosol eller på overf
Ny kemi opstår, når støv møder forureningRepræsentation af forureningshændelser, hvor mineralstøv og biomassebrændende røg blandes. Kredit:Hind Al-Abadleh Det er en ny kemi fundet at finde sted i en skydråbe, en våd aerosol eller på overf -
 Ny familie af selektive sølvbaserede kræftbekæmpende lægemidler opdagetEn familie af økonomiske sølvbaserede komplekser viser meget lovende resultater mod en række menneskelige kræftformer i laboratorietest, med meget lav toksicitet i rotteundersøgelser og minimale virkn
Ny familie af selektive sølvbaserede kræftbekæmpende lægemidler opdagetEn familie af økonomiske sølvbaserede komplekser viser meget lovende resultater mod en række menneskelige kræftformer i laboratorietest, med meget lav toksicitet i rotteundersøgelser og minimale virkn -
 Hvordan koncentration påvirker kemiske reaktionshastighederValentynVolkov/iStock/GettyImages Hvordan koncentration driver reaktionsrater I enhver kemisk transformation er hastigheden, hvormed produkter dannes, styret af hyppigheden af effektive kollisioner m
Hvordan koncentration påvirker kemiske reaktionshastighederValentynVolkov/iStock/GettyImages Hvordan koncentration driver reaktionsrater I enhver kemisk transformation er hastigheden, hvormed produkter dannes, styret af hyppigheden af effektive kollisioner m -
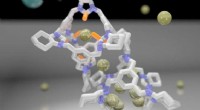 Burmolekyler fungerer som molekylsigter til adskillelse af brintisotopDannelse af en cocrystal forbedrer D2/H2-separationsydelsen. Kredit:University of Liverpool Et nyt hybridmateriale udviklet af forskere ved University of Liverpool kan bringe drømmen om kulstoffri
Burmolekyler fungerer som molekylsigter til adskillelse af brintisotopDannelse af en cocrystal forbedrer D2/H2-separationsydelsen. Kredit:University of Liverpool Et nyt hybridmateriale udviklet af forskere ved University of Liverpool kan bringe drømmen om kulstoffri
- Webb finder antydninger af en tredje planet på PDS 70
- Satellitdata finder top i en daglig lyncyklus
- Biology Primer:En begyndervejledning til grundlæggende begreber
- Klimaændringer gør nogle vulkanske faner mindre effektive til at reducere de globale temperaturer
- Forskere udvikler lagdelt koboltoxid med en rekordhøj termoelektrisk værdi
- Hvorfor er lysets lys så meget stærkere end nogen anden


