Svovls elektronkonfiguration:Forståelse af ydre skalelektroner
Her er hvorfor:
* Elektronkonfiguration: Svovls elektronkonfiguration er 1s² 2s² 2p⁶ 3s² 3p⁴.
* Ydre skal: Den yderste skal er den tredje skal (n=3).
* Yderste elektroner: 3s og 3p underniveauerne indeholder i alt 6 elektroner (2 i 3s og 4 i 3p).
Derfor har svovl 6 elektroner i sin ydre skal, hvilket gør det til et reaktivt grundstof.
Sidste artikelSvovls elektronkonfiguration:Forståelse af valenselektroner
Næste artikelKobberatomer Beregning:Hvor mange atomer i 8 gram?
 Varme artikler
Varme artikler
-
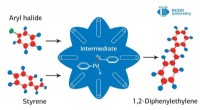 Kemiker udvikler blomsterlignende katalysatorer fra grafenKredit:RUDN University En RUDN -kemiker og kolleger fra Iran har udviklet en ny strategi til fremstilling af hule, porøse katalysatorer til Heck -koblingsreaktionen. Disse katalysatorer er kendete
Kemiker udvikler blomsterlignende katalysatorer fra grafenKredit:RUDN University En RUDN -kemiker og kolleger fra Iran har udviklet en ny strategi til fremstilling af hule, porøse katalysatorer til Heck -koblingsreaktionen. Disse katalysatorer er kendete -
 Forskere kaster lys over nyt billigt materiale til at se i mørketDr. Wendy Sarney bruger den molekylære stråleepitaximaskine ved US Army Research Laboratory til at producere infrarøde detektormaterialer med en ny synteseproces. Kredit:US Army Forskere ved U.S.
Forskere kaster lys over nyt billigt materiale til at se i mørketDr. Wendy Sarney bruger den molekylære stråleepitaximaskine ved US Army Research Laboratory til at producere infrarøde detektormaterialer med en ny synteseproces. Kredit:US Army Forskere ved U.S. -
 En praktisk guide til de seks kernetyper af kemiske reaktionerAf Lan Luo Opdateret 30. august 2022 Jardul/iStock/GettyImages Kemiske reaktioner er en integreret del af moderne teknologi og hverdagsliv – fra at drive motorer til at brygge drikkevarer. De drive
En praktisk guide til de seks kernetyper af kemiske reaktionerAf Lan Luo Opdateret 30. august 2022 Jardul/iStock/GettyImages Kemiske reaktioner er en integreret del af moderne teknologi og hverdagsliv – fra at drive motorer til at brygge drikkevarer. De drive -
 Personlig svedsensor overvåger pålideligt blodsukkeret uden fingerstikEn håndholdt enhed kombineret med en berøringssvedsensor (strimmel til højre) måler glukose i sved, mens en personlig algoritme konverterer disse data til et blodsukkerniveau. Kredit: ACS sensorer (2
Personlig svedsensor overvåger pålideligt blodsukkeret uden fingerstikEn håndholdt enhed kombineret med en berøringssvedsensor (strimmel til højre) måler glukose i sved, mens en personlig algoritme konverterer disse data til et blodsukkerniveau. Kredit: ACS sensorer (2


