Fluor vs. Jod:Forståelse af reaktivitetsforskelle
1. Mindre atomstørrelse: Fluor er meget mindre end jod. Det betyder, at elektronerne i den yderste skal er tættere på kernen og oplever en stærkere tiltrækning. Dette gør det lettere for fluor at få en elektron og danne en negativ ion.
2. Højere elektronegativitet: Fluor har den højeste elektronegativitet blandt alle elementer. Det betyder, at det har et stærkt træk på delte elektroner i en binding. Dette gør fluor mere tilbøjelige til at tiltrække elektroner fra andre atomer, hvilket fører til bindingsdannelse.
3. Svagere elektron-elektron frastødning: Med en mindre atomradius oplever elektronerne i fluors yderste skal mindre frastødning fra hinanden. Dette gør det lettere for fluor at tiltrække en ekstra elektron.
4. Fravær af d-orbitaler: Fluor, der er i den anden periode, mangler d-orbitaler. Dette begrænser dens evne til at udvide sin valensskal, hvilket gør den mere tilbøjelig til at danne en enkelt binding. Jod kan med sin større størrelse og tilstedeværelse af d-orbitaler danne flere bindinger.
5. Lavere bindingsdissociationsenergi: Bindingen mellem fluoratomer er svagere end bindingen mellem jodatomer. Dette gør det lettere at bryde fluor-fluor-bindingen og danne nye bindinger med andre grundstoffer.
Opsummering:
Fluors mindre størrelse, højere elektronegativitet, svagere elektron-elektron frastødning, fravær af d-orbitaler og lavere bindingsdissociationsenergi bidrager alle til dets høje reaktivitet sammenlignet med jod. Disse faktorer gør det lettere for fluor at få elektroner, danne bindinger og deltage i kemiske reaktioner.
 Varme artikler
Varme artikler
-
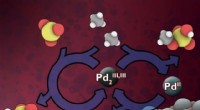 En ny måde at udnytte spildt metan påMIT kemiprofessor Yogesh Surendranath og tre kolleger har fundet en måde at bruge elektricitet på, som potentielt kan komme fra vedvarende kilder, at omdanne metan til derivater af methanol. Forskerne
En ny måde at udnytte spildt metan påMIT kemiprofessor Yogesh Surendranath og tre kolleger har fundet en måde at bruge elektricitet på, som potentielt kan komme fra vedvarende kilder, at omdanne metan til derivater af methanol. Forskerne -
 Højtemperaturenheder fremstillet af film, der bøjer, når de trækker vejret”Det mest interessante ved disse materialer er, at de fungerer ved temperaturer over 500 grader Celsius, ”Siger MIT -kandidatstuderende Jessica Swallow, afbildet med det udstyr, der bruges til at test
Højtemperaturenheder fremstillet af film, der bøjer, når de trækker vejret”Det mest interessante ved disse materialer er, at de fungerer ved temperaturer over 500 grader Celsius, ”Siger MIT -kandidatstuderende Jessica Swallow, afbildet med det udstyr, der bruges til at test -
 Spaghetti, vindueskarm, og LEGO:On-the-fly kompositmodelleringKredit:CC0 Public Domain Jo da, de er blandede metaforer - men ligesom modellering er et tæt skøn over processer i den virkelige verden, det samme er verbale forklaringer af en sådan nuanceret ari
Spaghetti, vindueskarm, og LEGO:On-the-fly kompositmodelleringKredit:CC0 Public Domain Jo da, de er blandede metaforer - men ligesom modellering er et tæt skøn over processer i den virkelige verden, det samme er verbale forklaringer af en sådan nuanceret ari -
 Ulovlig stofbrug kan være højere end hidtil antaget; svæver under særlige begivenhederKredit:CC0 Public Domain Amerikas narkotikaproblem kan være endnu værre, end embedsmænd er klar over. Og ulovlige stoffer indtages i højere grad under festlige begivenheder. Det er blot to af de k
Ulovlig stofbrug kan være højere end hidtil antaget; svæver under særlige begivenhederKredit:CC0 Public Domain Amerikas narkotikaproblem kan være endnu værre, end embedsmænd er klar over. Og ulovlige stoffer indtages i højere grad under festlige begivenheder. Det er blot to af de k


