Natrium og syrer:Forståelse af den farlige reaktion og sikkerhedsforanstaltninger
* Meget eksoterm reaktion: Reaktionen mellem natriummetal og fortyndede syrer (som saltsyre) er meget eksoterm, hvilket betyder, at den frigiver meget varme. Denne varme kan få den producerede brintgas til at antænde eksplosivt.
* Hurtig udvikling af brintgas: Reaktionen producerer brintgas (H2 ) hurtigt, hvilket fører til en opbygning af tryk. Dette kan få reaktionsbeholderen til at splintre eller eksplodere.
* Natriummetals reaktivitet: Natriummetal er ekstremt reaktivt og reagerer let med vand, som er til stede i de fleste fortyndede syrer. Dette øger reaktionens vold yderligere.
Sikkerhedsbekymringer:
* Brandfare: Den producerede brintgas er brandfarlig, og reaktionsvarmen kan let antænde den, hvilket fører til brand.
* Eksplosionsfare: Den hurtige gasudvikling og høje tryk kan forårsage en eksplosion, især hvis reaktionen ikke er ordentligt indeholdt.
* Natriummetalforbrændinger: Natriummetal reagerer med vand og luft, danner natriumhydroxid (NaOH) og frigiver varme. Dette kan forårsage alvorlige forbrændinger, hvis det kommer i kontakt med huden.
Alternativer:
I stedet for at reagere natriummetal med fortyndet syre, bruger kemikere sikrere alternativer:
* Reaktion med vand: Natriummetal kan sikkert reageres med vand, hvilket producerer hydrogengas og natriumhydroxid. Reaktionen er stadig eksoterm, men kan kontrolleres i laboratoriemiljø.
* Reaktion med ethanol: Natriummetal reagerer langsommere med ethanol og producerer hydrogengas og natriumethoxid. Denne reaktion er mindre eksoterm og sikrere at udføre.
Sammenfattende udgør den ekstreme reaktivitet af natriummetal med fortyndede syrer en alvorlig sikkerhedsrisiko, hvilket gør det upraktisk og usikkert at udføre sådanne reaktioner i typiske laboratoriemiljøer.
 Varme artikler
Varme artikler
-
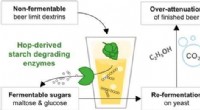 Humlet øl uden eksploderende flasker og for meget alkoholKredit:American Chemical Society Den glemte kunst at tør-hoppe øl for at forbedre smagen er tilbage på mode. Men denne praksis har undertiden uønskede bivirkninger, såsom et uventet højt alkoholin
Humlet øl uden eksploderende flasker og for meget alkoholKredit:American Chemical Society Den glemte kunst at tør-hoppe øl for at forbedre smagen er tilbage på mode. Men denne praksis har undertiden uønskede bivirkninger, såsom et uventet højt alkoholin -
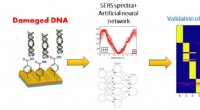 Forskere får neurale netværk til at opdage DNA-skader forårsaget af UV-strålingSkematisk diagram af SERS-sensorens drift i kombination med det neurale netværk til analyse af DNA-skader. Kredit:TPU Forskere ved Tomsk Polytekniske Universitet udførte sammen med Universitetet f
Forskere får neurale netværk til at opdage DNA-skader forårsaget af UV-strålingSkematisk diagram af SERS-sensorens drift i kombination med det neurale netværk til analyse af DNA-skader. Kredit:TPU Forskere ved Tomsk Polytekniske Universitet udførte sammen med Universitetet f -
 Partikelstørrelsen har betydning for porøse byggestenTynde (venstre) og tykke film lavet af porøse nanopartikler af calcium og silikat reagerede forskelligt under tryk som testet i et Rice University laboratorium. Partikler i de tynde film flyttede sig
Partikelstørrelsen har betydning for porøse byggestenTynde (venstre) og tykke film lavet af porøse nanopartikler af calcium og silikat reagerede forskelligt under tryk som testet i et Rice University laboratorium. Partikler i de tynde film flyttede sig -
 Ozonvandbehandling:Vigtigste ulemper og overvejelserRyan McVay/Photodisc/Getty Images Spildevand og spildevand indeholder en lang række mikroorganismer og organiske forurenende stoffer. Ozon bruges ofte til at fjerne disse forurenende stoffer, fordi d
Ozonvandbehandling:Vigtigste ulemper og overvejelserRyan McVay/Photodisc/Getty Images Spildevand og spildevand indeholder en lang række mikroorganismer og organiske forurenende stoffer. Ozon bruges ofte til at fjerne disse forurenende stoffer, fordi d
- På hvilket kontinent er Gobi -ørkenen?
- Hvad forstår du ved permuitit, hvordan er udmattet zeolit regenreret?
- Hvordan fugle skelner, hvor en bestemt lyd kommer fra
- Hvordan antager de fleste forskere, at solsystemet dannede sig?
- Antal elektroner i kulstof:En simpel forklaring
- En palæontolog, der underviser i anatomi, er god for medicin og videnskab


