Forståelse af krystalstruktur i ioniske forbindelser:En detaljeret forklaring
* Elektrostatisk attraktion: De modsatte ladninger af ioner tiltrækker hinanden stærkt. Denne tiltrækning er ansvarlig for dannelsen af ionbindingen og den samlede stabilitet af forbindelsen.
* Almindelig aftale: For at minimere frastødningen mellem ens ladninger og maksimere tiltrækning, arrangerer ionerne sig i en meget organiseret, tredimensionel gitterstruktur. Denne struktur er dikteret af ionernes størrelse og ladning.
* Gentagne enheder: Arrangementet af ioner gentages gennem hele krystallen og danner et regelmæssigt, gentaget mønster kaldet et krystalgitter. Denne gitterstruktur er grundlaget for den bestemte krystalform.
* Krystalflader: Det gentagne mønster af krystalgitteret resulterer i specifikke ionplaner, som kaldes krystalflader. Disse flader er de flade, glatte overflader, der definerer krystallens form.
* Forskellige krystalsystemer: Afhængigt af arrangementet af ioner i gitteret kan ioniske forbindelser krystallisere i forskellige krystalsystemer, såsom kubiske, tetragonale, hexagonale og andre. Hvert krystalsystem har et unikt sæt af vinkler og forhold mellem krystalfladerne, hvilket resulterer i distinkte krystalformer.
Eksempler:
* Natriumchlorid (NaCl): Danner kubiske krystaller, fordi natrium- og chloridionerne er arrangeret i et simpelt kubisk gitter.
* Kvarts (SiO2): Danner sekskantede krystaller på grund af det unikke arrangement af silicium og oxygenatomer.
Opsummering: Den stærke elektrostatiske tiltrækning mellem ioner tvinger dem til at arrangere sig i en specifik, gentagne gitterstruktur, hvilket fører til dannelsen af bestemte krystalformer. Størrelsen, ladningen og arrangementet af ioner bestemmer det særlige krystalsystem og den unikke form af den ioniske forbindelse.
 Varme artikler
Varme artikler
-
 Forskere bruger hele levende celler som skabeloner til at søge efter bioaktive molekylerHuman lungeadeconarcinomcelle brugt i denne forskning. Kredit:Daniel Carbajo En undersøgelse udført af forskere ved Institute for Advanced Chemistry of Catalonia (IQAC) fra det spanske nationale f
Forskere bruger hele levende celler som skabeloner til at søge efter bioaktive molekylerHuman lungeadeconarcinomcelle brugt i denne forskning. Kredit:Daniel Carbajo En undersøgelse udført af forskere ved Institute for Advanced Chemistry of Catalonia (IQAC) fra det spanske nationale f -
 Video:Hvad skal der til for at forvandle Boston havn til te?Kredit:The American Chemical Society Den 16. december 1773, demonstranterne i Bostons tefest smed mere end 340 kister fulde af te – svarende til omkring 18 og en halv million teposer – ind i havne
Video:Hvad skal der til for at forvandle Boston havn til te?Kredit:The American Chemical Society Den 16. december 1773, demonstranterne i Bostons tefest smed mere end 340 kister fulde af te – svarende til omkring 18 og en halv million teposer – ind i havne -
 Forskere finder tegn på proteinfoldning på stedet for intracellulære dråberKredit: Kemisk videnskab (2020). DOI:10.1039/D0SC04993J Forskere har opdaget det første tegn på proteinfoldning drevet af væske-væskefaseseparation, et fænomen, hvor væsker dannes til mikroskopis
Forskere finder tegn på proteinfoldning på stedet for intracellulære dråberKredit: Kemisk videnskab (2020). DOI:10.1039/D0SC04993J Forskere har opdaget det første tegn på proteinfoldning drevet af væske-væskefaseseparation, et fænomen, hvor væsker dannes til mikroskopis -
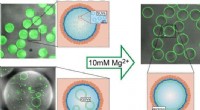 Cellelignende lipidvesikler, som kan udfyldes med naturlige celleproteinerLipidvesikler (til venstre:LUVer eller GUVer; grøn) blev indkapslet i copolymerstabiliserede dråber. Vesiklerne kan transformeres til et lipid-dobbeltlag ved den copolymerstabiliserede dråbe indre græ
Cellelignende lipidvesikler, som kan udfyldes med naturlige celleproteinerLipidvesikler (til venstre:LUVer eller GUVer; grøn) blev indkapslet i copolymerstabiliserede dråber. Vesiklerne kan transformeres til et lipid-dobbeltlag ved den copolymerstabiliserede dråbe indre græ
- Hvilket vand, der bevæger sig over jordoverfladen?
- Hvad er sporene på DNA-dobbelthelixen der er lavet af?
- Hvad er kemisk sammensætning af atmosfære?
- En gas udøver et tryk på 0,892 atm i 5,00 L -beholder ved 15 grader celsius densiteten er 1,22 GL …
- Hvordan dannes vand gennem naturlige processer?
- Hvad er hårdhed af CZ og zirkon?


