Bevaringslove i kemiske reaktioner:Hvad forbliver konstant?
* Samlet masse: Dette er det grundlæggende princip for bevarelse af masse . Den samlede masse af reaktanterne (udgangsmaterialerne) skal svare til den samlede masse af produkterne (det der er dannet). Atomer bliver ikke skabt eller ødelagt, bare omarrangeret.
* Antal atomer: Mens arrangementet af atomer ændres, forbliver det samlede antal af hver type atom det samme. Dette er også relateret til bevarelse af masse.
* Samlet energi: Dette er princippet om bevarelse af energi . Energi kan omdannes fra en form til en anden (som kemisk energi til varme), men den kan ikke skabes eller ødelægges.
Følgende ting ændrer sig dog under en kemisk reaktion:
* Kemisk sammensætning: Stoffernes kemiske sammensætning ændres i takt med, at der dannes nye forbindelser.
* Fysiske egenskaber: Egenskaber som smeltepunkt, kogepunkt, farve og massefylde kan ændre sig drastisk, efterhånden som nye stoffer dannes.
* Sagens tilstand: Den fysiske tilstand af reaktanterne og produkterne kan ændre sig (f.eks. fra væske til gas).
Fortæl mig, hvis du gerne vil udforske nogen af disse begreber yderligere!
Sidste artikelReaktion af HCl og zink:Produkter og kemisk ligning
Næste artikelForståelse af salte:binære ioniske forbindelser og mere
 Varme artikler
Varme artikler
-
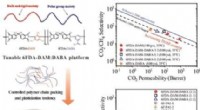 Polyimidmembraner til rensning af naturgasKredit:Wiley Naturgas, der indeholder større mængder hydrogensulfid (H 2 S) og kuldioxid (CO 2 ) kaldes sur gas. Før det kan komme ind i en pipeline, det skal sødes ved at fjerne dets sure ure
Polyimidmembraner til rensning af naturgasKredit:Wiley Naturgas, der indeholder større mængder hydrogensulfid (H 2 S) og kuldioxid (CO 2 ) kaldes sur gas. Før det kan komme ind i en pipeline, det skal sødes ved at fjerne dets sure ure -
 Test af designet kulstofmaterialer til at rense spildevandKredit:CC0 Public Domain Affaldsstrømme fra industri og landbrug kunne bruges til produktion af kul, der kan tjene som en billig adsorbent til vandrensning. I sit speciale på Industridoktoralskole
Test af designet kulstofmaterialer til at rense spildevandKredit:CC0 Public Domain Affaldsstrømme fra industri og landbrug kunne bruges til produktion af kul, der kan tjene som en billig adsorbent til vandrensning. I sit speciale på Industridoktoralskole -
 Konstrueret insulin, der kan aktiveres af forhøjet blodsukker, kan forbedre diabetikernes livskvali…“[Glukose-responsiv insulin] har været et mangeårigt mål for diabetesområdet, ”Siger professor Michael Strano. Hvis det gøres korrekt, du kunne gøre det, så diabetikere lejlighedsvis kunne tage en dos
Konstrueret insulin, der kan aktiveres af forhøjet blodsukker, kan forbedre diabetikernes livskvali…“[Glukose-responsiv insulin] har været et mangeårigt mål for diabetesområdet, ”Siger professor Michael Strano. Hvis det gøres korrekt, du kunne gøre det, så diabetikere lejlighedsvis kunne tage en dos -
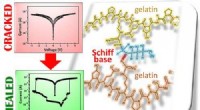 Selvreparerende gelatinebaseret film kan være et smart træk for elektronikKredit:American Chemical Society At tabe en mobiltelefon kan nogle gange forårsage overfladiske revner. Men andre gange, enheden kan helt stoppe med at fungere, fordi der udvikles brud i det mater
Selvreparerende gelatinebaseret film kan være et smart træk for elektronikKredit:American Chemical Society At tabe en mobiltelefon kan nogle gange forårsage overfladiske revner. Men andre gange, enheden kan helt stoppe med at fungere, fordi der udvikles brud i det mater
- Kan alle organismer gengive ved hjælp af celledeling?
- Tetrahedralitet er nøglen til det unikke ved vand
- Hvad er et legitimt stjerne-register?
- Hvordan ændres tyngdekraften mellem to genstande, når afstand dem halveres?
- Hvorfor er de lettere farvede halvdele af måne og jord altid mod solen?
- Hvilken proces involverer sammenligning af klippelag med andre i en sekvens for at bestemme dens ald…


