Redox-reaktioner, forbrænding, syntese, nedbrydning og dobbeltforskydning:En omfattende guide
1. Redox-reaktioner:
* Definition: Reaktioner, der involverer overførsel af elektroner. En art bliver oxideret (taber elektroner), mens en anden bliver reduceret (vinder elektroner).
* Eksempel: Afbrænding af metan (CH4) i oxygen til dannelse af kuldioxid (CO2) og vand (H2O).
2. Forbrændingsreaktioner:
* Definition: En hurtig reaktion mellem et stof og en oxidant (normalt oxygen), der producerer varme og lys.
* Eksempel: Afbrænding af træ.
3. Enkelt-erstatningsreaktioner:
* Definition: Et grundstof erstatter et andet grundstof i en forbindelse.
* Eksempel: Zink (Zn) reagerer med saltsyre (HCl) for at producere zinkchlorid (ZnCl2) og hydrogengas (H2).
4. Syntesereaktioner:
* Definition: To eller flere reaktanter kombineres for at danne et enkelt produkt.
* Eksempel: Natrium (Na) reagerer med klor (Cl2) til dannelse af natriumchlorid (NaCl).
5. Nedbrydningsreaktioner:
* Definition: En enkelt reaktant nedbrydes i to eller flere produkter.
* Eksempel: Nedbrydning af calciumcarbonat (CaCO3) til calciumoxid (CaO) og kuldioxid (CO2).
6. Dobbelt-erstatningsreaktioner:
* Definition: De positive og negative ioner af to reaktanter skifter plads.
* Eksempel: Reaktionen af sølvnitrat (AgNO3) og natriumchlorid (NaCl) til dannelse af sølvchlorid (AgCl) og natriumnitrat (NaNO3).
Svaret:
De to reaktioner, der passer til kriterierne for at være både redox- og forbrændingsreaktioner, er:
1. Forbrændingsreaktioner: Alle forbrændingsreaktioner involverer overførsel af elektroner, hvilket gør dem til redoxreaktioner.
2. Nogle enkelt-erstatningsreaktioner: Visse enkeltudskiftningsreaktioner kan betragtes som redoxreaktioner og forbrændingsreaktioner, hvis reaktionen involverer oxygen som reaktant, der udskiftes. For eksempel:
* 2Mg(s) + O2(g) → 2MgO(s) Her reagerer magnesium (Mg) med ilt (O2) og danner magnesiumoxid (MgO), hvilket frigiver varme og lys.
Vigtig bemærkning: Ikke alle enkeltudskiftningsreaktioner er forbrændingsreaktioner. Forbrænding involverer specifikt hurtig reaktion med ilt.
 Varme artikler
Varme artikler
-
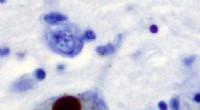 Ny enzymnøgle til bedre behandling af Parkinsons sygdomImmunhistokemi for alfa-synuclein, der viser positiv farvning (brun) af et intraneuralt Lewy-legeme i Substantia nigra ved Parkinsons sygdom. Kredit:Wikipedia Forskere har opdaget et nyt enzym, de
Ny enzymnøgle til bedre behandling af Parkinsons sygdomImmunhistokemi for alfa-synuclein, der viser positiv farvning (brun) af et intraneuralt Lewy-legeme i Substantia nigra ved Parkinsons sygdom. Kredit:Wikipedia Forskere har opdaget et nyt enzym, de -
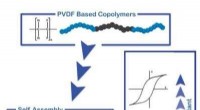 Ferroelektriske polymerer gjort mere alsidigeEn blokcopolymer af PVDF (sort) og en isolerende polymerkæde (blå) danner en blokcopolymer. Gennem faseadskillelse, blokkene samles i film. De dielektriske egenskaber kan indstilles ved at variere sam
Ferroelektriske polymerer gjort mere alsidigeEn blokcopolymer af PVDF (sort) og en isolerende polymerkæde (blå) danner en blokcopolymer. Gennem faseadskillelse, blokkene samles i film. De dielektriske egenskaber kan indstilles ved at variere sam -
 Ledende papir kunne muliggøre fremtidig fleksibel elektronikForskere laver ledende papir ved at belægge det med en ionisk gel. Kredit:American Chemical Society Roll-up computerskærme og anden fleksibel elektronik kommer tættere på virkeligheden, efterhånde
Ledende papir kunne muliggøre fremtidig fleksibel elektronikForskere laver ledende papir ved at belægge det med en ionisk gel. Kredit:American Chemical Society Roll-up computerskærme og anden fleksibel elektronik kommer tættere på virkeligheden, efterhånde -
 Forskere opdager en effektiv og bæredygtig måde at filtrere salt- og metalioner fra vand påKredit:CC0 Public Domain Med to milliarder mennesker verden over mangler adgang til rent og sikkert drikkevand, fælles forskning fra Monash University, CSIRO og University of Texas i Austin offent
Forskere opdager en effektiv og bæredygtig måde at filtrere salt- og metalioner fra vand påKredit:CC0 Public Domain Med to milliarder mennesker verden over mangler adgang til rent og sikkert drikkevand, fælles forskning fra Monash University, CSIRO og University of Texas i Austin offent
- Luskede hanner adopterer kvindelignende hjerner for at narre store dyr
- Sikkerhedsscreening af nanomaterialer kan blive hurtigere, billigere med ny laboratorietest
- Hvad er det andet navn på tidevandsbølge?
- 57 kilo er hvor mange pund?
- Hvordan får du brintgas fra silicium og vand?
- Proof-of-concept undersøgelse viser, hvordan human insulin kan produceres i komælk


