HCl vs. CH3COOH:Forståelse af ioniseringsgrader - kemi forklaret
HCl (saltsyre)
* Stærk syre: HCl er en stærk syre, hvilket betyder, at den ioniserer næsten fuldstændigt i vand.
* Høj grad af ionisering: I opløsning donerer HCl let sin proton (H+) til vand, hvilket producerer H3 O+ (hydroniumion) og Cl- (chloridion). Ligevægten ligger tungt mod den ioniserede form.
* I det væsentlige 100 % ioniseret: Vi anser typisk HCl for at være 100% ioniseret i fortyndede vandige opløsninger.
CH3 COOH (eddikesyre)
* Svag syre: Eddikesyre er en svag syre, hvilket betyder, at den kun ioniseres delvist i vand.
* Lav ioniseringsgrad: Kun en lille del af eddikesyremolekylerne donerer deres proton til vand og danner H3 O+ og CH3 COO- (acetation). Ligevægten favoriserer den ikke-ioniserede form.
* Begrænset ionisering: Eddikesyre når en ligevægt, hvor en lille, men betydelig del forbliver i sin molekylære form.
Nøgleforskelle
* Styrke: HCl er en stærk syre, mens CH3 COOH er en svag syre.
* Ioniseringsprocent: HCl ioniserer næsten fuldstændigt (tæt på 100%), mens CH3 COOH ioniserer kun delvist.
* Ligevægt: Ligevægten for HCl ligger tungt mod den ioniserede form, hvorimod ligevægten for CH3 COOH favoriserer den ikke-ioniserede form.
Opsummering:
HCl har en meget højere grad af ionisering end CH3 COOH på grund af sin natur som en stærk syre. Det betyder, at en opløsning af HCl vil indeholde væsentligt flere H+ ioner end en opløsning af eddikesyre i samme koncentration.
 Varme artikler
Varme artikler
-
 Video:Sådan spotter du falske metaller med syrerKredit:The American Chemical Society Syrer er reaktive, med selv svage syrer som eddike, der interagerer med andre materialer for at imponere eleverne. Men stærke syrer kan virkelig vise sig. For
Video:Sådan spotter du falske metaller med syrerKredit:The American Chemical Society Syrer er reaktive, med selv svage syrer som eddike, der interagerer med andre materialer for at imponere eleverne. Men stærke syrer kan virkelig vise sig. For -
 Enzym fra briny dyb genopstod i laboratorietRosetprøveudtageren bruges til at indsamle bakterieprøverne fra saltvandspuljen i Det Røde Hav. Kredit:André Antunes, Edge Hill University, Storbritannien. Mystiske mikrober, der trives i varme og
Enzym fra briny dyb genopstod i laboratorietRosetprøveudtageren bruges til at indsamle bakterieprøverne fra saltvandspuljen i Det Røde Hav. Kredit:André Antunes, Edge Hill University, Storbritannien. Mystiske mikrober, der trives i varme og -
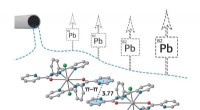 Kemikere foreslår nye reagenser til fjernelse af bly fra spildevandKredit:RUDN University RUDN -universitetets kemikere har sammen med kolleger fra andre lande syntetiseret nye forbindelser, der effektivt binder blyioner og kan bruges til at fjerne det fra spilde
Kemikere foreslår nye reagenser til fjernelse af bly fra spildevandKredit:RUDN University RUDN -universitetets kemikere har sammen med kolleger fra andre lande syntetiseret nye forbindelser, der effektivt binder blyioner og kan bruges til at fjerne det fra spilde -
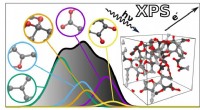 En model trænet til at forudsige spektroskopiske profiler hjælper med at tyde strukturen af mate…Den nye algoritme forudsiger XPS-spektrene for komplekse materialer baseret på individuelle atomare bidrag. Kredit:Miguel Caro / Aalto University Kulstofbaserede materialer rummer et enormt potenti
En model trænet til at forudsige spektroskopiske profiler hjælper med at tyde strukturen af mate…Den nye algoritme forudsiger XPS-spektrene for komplekse materialer baseret på individuelle atomare bidrag. Kredit:Miguel Caro / Aalto University Kulstofbaserede materialer rummer et enormt potenti
- Hvad er det fysiske begreb om kraftfriktion og masse?
- Forskere udvikler principper for oprettelse af en akustisk diode
- Hvad er den fulde form for NC med hensyn til ISO?
- Rusland afviser, at de mistænker amerikanske astronauter for at bore hul på rumstationen
- Hvordan adskiller erosion sig fra deponering?
- Hvor har vand den mest kinetiske energi?


