Kobbersulfat- og ammoniakreaktion:Kemi og observationer
1. Dannelse af en dyb blå løsning:
* Indledningsvis, efter tilsætning af ammoniak til en opløsning af kobbersulfat, et lyseblåt bundfald af kobberhydroxid (Cu(OH)2 ) formularer:
CuSO4 (aq) + 2NH3 (aq) + 2H2 O(l) → Cu(OH)2 (s) + (NH4 )2 SO4 (aq)
* Efterhånden som mere ammoniak tilsættes, opløses bundfaldet og danner en dybblå opløsning. Dette skyldes dannelsen af tetraamminkobber(II)-kompleksionen ([Cu(NH3 )4 ] 2+ ):
Cu(OH)2 (s) + 4NH3 (aq) → [Cu(NH3 )4 ] 2+ (vandig) + 2OH - (aq)
2. Dannelse af andre komplekser:
* Reaktionen med ammoniak stopper ikke der. Afhængigt af koncentrationen af ammoniak kan der dannes andre kobber-ammoniakkomplekser, herunder:
* [Cu(NH3 )] 2+
* [Cu(NH3 )2 ] 2+
* [Cu(NH3 )3 ] 2+
Nøgleobservationer:
* Farveændring: Opløsningen bliver fra lyseblå (kobbersulfat) til dybblå ([Cu(NH3 )4 ] 2+ ).
* Bundfaldsdannelse og opløsning: Til at begynde med dannes et lyseblåt bundfald, som derefter opløses ved tilsætning af mere ammoniak.
Vigtig bemærkning:
* Dannelsen af disse kobber-ammoniakkomplekser er et eksempel på ligandudvekslingsreaktioner , hvor ammoniakmolekyler erstatter vandmolekyler koordineret til kobberionen.
* Stabiliteten af disse komplekser afhænger af koncentrationen af ammoniak og opløsningens pH.
Denne reaktion er et klassisk eksempel på overgangsmetallers alsidige kemi og deres evne til at danne komplekser med forskellige ligander.
Sidste artikelHCl:syre eller base? Forstå dens egenskaber
Næste artikelMetaloxidation:Produkter dannet, når metaller reagerer med ilt
 Varme artikler
Varme artikler
-
 Hurtige og pålidelige tests for legionellabakterier i vandKredit:Giovanni Cancemi, Shutterstock En fuldautomatisk testanordning kan nu installeres på vandsteder, der er mistænkt for forurening med legionella-bakterier. Enheden lover mere pålidelige resul
Hurtige og pålidelige tests for legionellabakterier i vandKredit:Giovanni Cancemi, Shutterstock En fuldautomatisk testanordning kan nu installeres på vandsteder, der er mistænkt for forurening med legionella-bakterier. Enheden lover mere pålidelige resul -
 Optisk påvisning af flere bakteriearter ved hjælp af metal-organiske hybrider i nanometerskalaGrafisk abstrakt. Kredit:Analytisk kemi (2022). DOI:10.1021/acs.analchem.2c01188 Forskere fra Osaka Metropolitan University har udviklet en enkel, hurtig metode til samtidigt at identificere flere
Optisk påvisning af flere bakteriearter ved hjælp af metal-organiske hybrider i nanometerskalaGrafisk abstrakt. Kredit:Analytisk kemi (2022). DOI:10.1021/acs.analchem.2c01188 Forskere fra Osaka Metropolitan University har udviklet en enkel, hurtig metode til samtidigt at identificere flere -
 Forskerteam udvikler en ny klasse bløde materialerShifeng Nian og ph.d. studerende Jinchang Zhu ilægger blækket i en sprøjte til 3D -print. Kredit:University of Virginia Jeg tror, du er stille. Dette var den mest brugte sætning i 2020, ifølge H
Forskerteam udvikler en ny klasse bløde materialerShifeng Nian og ph.d. studerende Jinchang Zhu ilægger blækket i en sprøjte til 3D -print. Kredit:University of Virginia Jeg tror, du er stille. Dette var den mest brugte sætning i 2020, ifølge H -
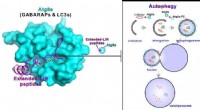 Forskere opdager autofagi-hæmmende peptider fra gigantiske ankyrinerDette visuelle abstrakt præsenterer de superstærke Atg8s-bindende peptider, der effektivt kan hæmme autofagi. Kredit:Division of Life Science, HKUST Autofagi, betyder selvspisning på græsk, er en
Forskere opdager autofagi-hæmmende peptider fra gigantiske ankyrinerDette visuelle abstrakt præsenterer de superstærke Atg8s-bindende peptider, der effektivt kan hæmme autofagi. Kredit:Division of Life Science, HKUST Autofagi, betyder selvspisning på græsk, er en
- Kombination af grundstofferne palladium og ruthenium til industrien
- Den mindste magnetfeltsensor i verden udviklet
- Sådan beregnes J-koblingskonstanter
- Sådan fungerer dampskovle
- Hvor hurtigt rejser en person i rummet, når den er uden for rumfartøjet?
- Hvilken art er bedst egnet til livet? Alle har lige chancer, siger videnskabsmænd


