Kaliumchloridsyntese:Kemisk ligning og nedbrydning af reaktioner
2K(s) + Cl2(g) → 2KCl(s)
Her er en opdeling af ligningen:
* 2K(s): Dette repræsenterer to mol fast kalium (K). "(erne)" angiver, at den er i fast tilstand.
* Cl2(g): Dette repræsenterer et mol chlorgas (Cl2). "(g)" angiver, at den er i gasform.
* 2KCl(s): Dette repræsenterer to mol fast kaliumchlorid (KCl). "(erne)" angiver, at den er i fast tilstand.
Forklaring:
Dette er en kraftig reaktion, hvor kalium let taber en elektron for at blive en positiv ion (K⁺), og klor får en elektron til at blive en negativ ion (Cl⁻). Disse modsat ladede ioner tiltrækker derefter hinanden og danner den ioniske forbindelse kaliumchlorid (KCl).
 Varme artikler
Varme artikler
-
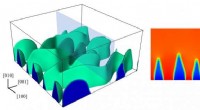 Ikke så hurtigt:Nogle batterier kan skubbes for langtTil venstre, en 3D-model af Rice Universitys materialeforskere viser en fasegrænse, da en delithierende lithiumjernphosphatkatode undergår hurtig afladning. Til højre, et tværsnit viser den fingerlign
Ikke så hurtigt:Nogle batterier kan skubbes for langtTil venstre, en 3D-model af Rice Universitys materialeforskere viser en fasegrænse, da en delithierende lithiumjernphosphatkatode undergår hurtig afladning. Til højre, et tværsnit viser den fingerlign -
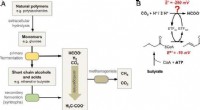 Afgørende trin identificeret i omdannelsen af biomasse til metanKredit:DOI:10.1073/pnas.2111682118 Mikrobiel produktion af metan fra organisk materiale er en væsentlig proces i det globale kulstofkredsløb og en vigtig kilde til vedvarende energi. Denne naturli
Afgørende trin identificeret i omdannelsen af biomasse til metanKredit:DOI:10.1073/pnas.2111682118 Mikrobiel produktion af metan fra organisk materiale er en væsentlig proces i det globale kulstofkredsløb og en vigtig kilde til vedvarende energi. Denne naturli -
 Næste generations opløsningsmidler fanger kulstof med halvdelen af energienPacific Northwest National Laboratory -videnskabsmand David Heldebrant fanger svovl og kuldioxid fra testemissionsstrømme i en proces kaldet Reversible Acid Gas Capture. Kredit:Pacific Northwest Natio
Næste generations opløsningsmidler fanger kulstof med halvdelen af energienPacific Northwest National Laboratory -videnskabsmand David Heldebrant fanger svovl og kuldioxid fra testemissionsstrømme i en proces kaldet Reversible Acid Gas Capture. Kredit:Pacific Northwest Natio -
 Kompositmetalskum tager varmen, rykke tættere på udbredte applikationerStål-stål kompositmetalskumprøver før test (højre) og efter 100 minutters eksponering for 825C (venstre). Kredit:Afsaneh Rabiei, NC State University Forskere fra North Carolina State University ha
Kompositmetalskum tager varmen, rykke tættere på udbredte applikationerStål-stål kompositmetalskumprøver før test (højre) og efter 100 minutters eksponering for 825C (venstre). Kredit:Afsaneh Rabiei, NC State University Forskere fra North Carolina State University ha
- Hvad holder et atom holdt sammen?
- Billede:NASAs SDO opdager en månetransit
- Rørene bag et køleskab er varme Hvor kommer energien fra til disse rør?
- Forskere løser seismisk mysterium, der rystede det centrale Alberta-samfund
- Hvordan forvandler du atomenergi til termisk energi?
- Hvordan former vi som mennesker jorden sammen med naturlige kræfter?


