Overgangsmetaller:egenskaber, karakteristika og eksempler
Her er nogle nøglekarakteristika ved overgangsmetaller:
Egenskaber:
* Variable oxidationstilstande: De kan danne ioner med flere positive ladninger på grund af tilstedeværelsen af d elektroner.
* Farvede forbindelser: Mange danner farvestrålende forbindelser på grund af de d-d elektronovergange, der opstår, når lys interagerer med metalionerne.
* Gode ledere af varme og elektricitet: De har frie elektroner i deres d-orbitaler, hvilket giver mulighed for effektiv ledning.
* Magnetiske egenskaber: Nogle er magnetiske, mens andre ikke er det på grund af arrangementet af elektroner i deres d-orbitaler.
* Katalytisk aktivitet: Mange er fremragende katalysatorer, der fremmer kemiske reaktioner uden at blive forbrugt.
Eksempler:
* Jern (Fe): Anvendes i stål og andre legeringer.
* Kobber (Cu): Anvendes i elektriske ledninger og VVS.
* Guld (Au): Et ædelmetal, der bruges i smykker og elektronik.
* Titanium (Ti): Et stærkt og let metal brugt i rumfart og medicinske implantater.
* Chromium (Cr): Anvendes i rustfrit stål og som belægning for korrosionsbestandighed.
Hvorfor kaldes de "overgangsmetaller"?
De kaldes "overgangs"-metaller, fordi deres egenskaber er mellem egenskaberne for de meget reaktive alkalimetaller og jordalkalimetaller på venstre side af det periodiske system og ikke-metallerne på højre side. De udviser en overgang i egenskaber og udviser karakteristika for både metallisk og ikke-metallisk adfærd.
Bemærk:
Der er nogle undtagelser fra den generelle definition af overgangsmetaller. For eksempel betragtes scandium (Sc) og zink (Zn) nogle gange som overgangsmetaller, selvom de strengt taget ikke opfylder kriterierne.
 Varme artikler
Varme artikler
-
 Kemisk festende bakterier fjerner sandsynligt kræftfremkaldende stof fra forurenet vandKredit:New Jersey Institute of Technology Selvom det ikke fremgår af de fleste produktingrediensetiketter, den organiske kemiske stabilisator og fremstillingsbiprodukt, 1, 4-dioxan, kan findes i u
Kemisk festende bakterier fjerner sandsynligt kræftfremkaldende stof fra forurenet vandKredit:New Jersey Institute of Technology Selvom det ikke fremgår af de fleste produktingrediensetiketter, den organiske kemiske stabilisator og fremstillingsbiprodukt, 1, 4-dioxan, kan findes i u -
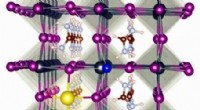 Et komplet sæt energiniveaupositioner for alle primære metalhalogenidperovskitterKredit:Eindhoven University of Technology Metalhalogenidperovskitter udgør en populær klasse af materialer med spændende optoelektroniske egenskaber. En grundlæggende forståelse af variationerne i
Et komplet sæt energiniveaupositioner for alle primære metalhalogenidperovskitterKredit:Eindhoven University of Technology Metalhalogenidperovskitter udgør en populær klasse af materialer med spændende optoelektroniske egenskaber. En grundlæggende forståelse af variationerne i -
 At træne får hydrogeler til at fungere mere som musklerEn mekanisk trænet kunstig muskel modstår beskadigelse (revne) forplantning ved hjælp af justerede nanofibriller, en lignende træthedsbestandig mekanisme som i skeletmuskler. Kredit:Ji Liu, Shaoting L
At træne får hydrogeler til at fungere mere som musklerEn mekanisk trænet kunstig muskel modstår beskadigelse (revne) forplantning ved hjælp af justerede nanofibriller, en lignende træthedsbestandig mekanisme som i skeletmuskler. Kredit:Ji Liu, Shaoting L -
 Forskere bringer polymerer i fokus på atomskalaEn gengivelse (grå og pink) af den molekylære struktur af en peptoid polymer, der blev undersøgt af et team ledet af Berkeley Lab og UC Berkeley. Holdets succes med at afbilde polymerers struktur i at
Forskere bringer polymerer i fokus på atomskalaEn gengivelse (grå og pink) af den molekylære struktur af en peptoid polymer, der blev undersøgt af et team ledet af Berkeley Lab og UC Berkeley. Holdets succes med at afbilde polymerers struktur i at
- Kan du bruge en 250V 15 amp sikring til 125V amp?
- Menneskets knoglestørrelse og struktur er et resultat af miljøet og?
- Cocrystal engineering:En teknik til at designe multifunktionelle materialer
- Europa opfordrede til at tackle flaskehalse i luftrummet, da forsinkelser stiger
- Er der luft på Planet Mars?
- Hvad er adverb til udforskning?


