Polære kovalente bindinger:definition, elektronegativitet og eksempler
Her er en oversigt:
* Kovalent binding: En kovalent binding dannes, når to atomer deler et elektronpar.
* Polar: Udtrykket "polær" henviser til den ujævne fordeling af elektrontæthed i bindingen.
* Elektronegativitet: Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner i en kemisk binding.
Sådan virker det:
Når to atomer med forskellige elektronegativiteter danner en binding, vil atomet med den højere elektronegativitet trække de delte elektroner tættere på sig selv. Dette skaber en delvis negativ ladning (δ-) på det mere elektronegative atom og en delvis positiv ladning (δ+) på det mindre elektronegative atom.
Eksempel:
Overvej vandmolekylet (H2O). Ilt har en højere elektronegativitet end brint. Som et resultat bliver de delte elektroner trukket tættere på oxygenatomet, hvilket giver det en delvis negativ ladning (δ-). Hydrogenatomerne, der har en delvis positiv ladning (δ+), tiltrækkes af oxygenatomet. Dette skaber en polær kovalent binding, og vandmolekylet som helhed bliver et polært molekyle.
Nøglekarakteristika:
* Ulige deling af elektroner: Elektroner deles ikke ligeligt mellem atomerne.
* Delvis afgifter: Atomerne involveret i bindingen udvikler delvise positive og delvise negative ladninger.
* Dipolmoment: Polære kovalente bindinger skaber et dipolmoment, som er et mål for adskillelsen af ladning i et molekyle.
* Opløselighed: Polære kovalente molekyler har tendens til at være opløselige i polære opløsningsmidler som vand.
I modsætning til ikke-polære kovalente bindinger:
I ikke-polære kovalente bindinger deles elektronerne ligeligt mellem atomerne, fordi atomerne har lignende elektronegativitet. Dette resulterer i ingen delladninger og intet dipolmoment. Eksempler inkluderer bindingerne i diatomiske molekyler som O₂ og N₂.
 Varme artikler
Varme artikler
-
 Kan citronsyre være et grønt alternativ til beskyttelse af stål?Citronsyre som grønt alternativ til metalbeskyttelsesmiddel. Kredit:European Space Agency Salpetersyre er i øjeblikket den mest anvendte passiveringsløsning til beskyttelse af rustfrit stål mod ko
Kan citronsyre være et grønt alternativ til beskyttelse af stål?Citronsyre som grønt alternativ til metalbeskyttelsesmiddel. Kredit:European Space Agency Salpetersyre er i øjeblikket den mest anvendte passiveringsløsning til beskyttelse af rustfrit stål mod ko -
 Test af smartphones tester forgiftet vandrisiko for millioner af livEn smartphone -enhed kan hjælpe millioner af mennesker med at undgå drikkevand, der er forurenet af arsen. Forskere har udviklet en biosensor, der tilsluttes en telefon og bruger bakterier til at opd
Test af smartphones tester forgiftet vandrisiko for millioner af livEn smartphone -enhed kan hjælpe millioner af mennesker med at undgå drikkevand, der er forurenet af arsen. Forskere har udviklet en biosensor, der tilsluttes en telefon og bruger bakterier til at opd -
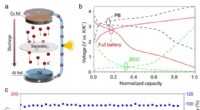 Konstruktion af kulstofbaserede celle-lignende kugler til robust kaliumanode(a) Skematisk illustration af K-ion-fuldbatteriet baseret på det forberedte BCC og Preussisk blå (PB). (b) Opladningsafladningsprofiler for halvbatteriet og fuldt batteri. (c) Cykelstabilitet ved 500
Konstruktion af kulstofbaserede celle-lignende kugler til robust kaliumanode(a) Skematisk illustration af K-ion-fuldbatteriet baseret på det forberedte BCC og Preussisk blå (PB). (b) Opladningsafladningsprofiler for halvbatteriet og fuldt batteri. (c) Cykelstabilitet ved 500 -
 Forskning afdækker potentiel bæredygtig raffineringsmetode for ligninKredit:CC0 Public Domain Lignin, bruges som en vedvarende ressource til at producere produkter af høj værdi, har givet både produktionsmæssige og økonomiske udfordringer for bioraffinaderidriften.
Forskning afdækker potentiel bæredygtig raffineringsmetode for ligninKredit:CC0 Public Domain Lignin, bruges som en vedvarende ressource til at producere produkter af høj værdi, har givet både produktionsmæssige og økonomiske udfordringer for bioraffinaderidriften.
- Hvilken slags energi har pinden en kamp?
- Hvad er modstand mod bevægelsen af et objekt?
- Hvor bredt tilgængelig er brint?
- Fremme af beskrivelsen af mystisk vand for at forbedre lægemiddeldesign
- Vi flyver Kongressen:Hvordan flyselskaber skjult lobbyer politikere
- Bradley Fighting Hvordan køretøjer fungerer


