Elektronacceptorer:Forståelse af ikke-metaller og deres rolle
Her er hvorfor:
* Elektronkonfiguration: Ikke-metaller har et højt antal elektroner i deres ydre skal (valensskal). De har en tendens til at have næsten fulde valensskaller, hvilket gør dem ivrige efter at få elektroner for at opnå en stabil oktet (8 elektroner) eller duet (2 elektroner) konfiguration.
* Elektronegativitet: Ikke-metaller har generelt højere elektronegativitet end metaller. Elektronegativitet er et atoms evne til at tiltrække elektroner i en kemisk binding. Dette betyder, at ikke-metaller er mere tilbøjelige til at tiltrække elektroner fra andre atomer, hvilket gør dem til acceptorer.
Her er nogle eksempler på elementer, der let accepterer elektroner:
* Halogener (Gruppe 17): Fluor (F), klor (Cl), brom (Br), jod (I) og astatin (At). Disse er de mest reaktive ikke-metaller og får let en elektron for at opnå en stabil oktetkonfiguration.
* Oxygen (O): Ilt er meget elektronegativt og får normalt to elektroner til at danne en stabil oxidion (O²⁻).
* Svovl (S): Svovl kan få to elektroner til at danne en sulfidion (S²⁻).
* Nitrogen (N): Nitrogen kan få tre elektroner til at danne en nitridion (N³⁻).
Det er vigtigt at bemærke, at den lethed, hvormed et grundstof accepterer elektroner, er påvirket af dets placering i det periodiske system og dets kemiske miljø.
 Varme artikler
Varme artikler
-
 Forskning i brugsklar terapeutisk mad søger drastisk reduktion af dødsfald som følge af alvorlig …MIT kandidatstuderende Tonghan Gu (til højre) arbejder med teknikere på en facilitet i Vasai, Indien, at producere et parti brugsklare terapeutiske fødevarer i pulverform. Formlen, han har udviklet, b
Forskning i brugsklar terapeutisk mad søger drastisk reduktion af dødsfald som følge af alvorlig …MIT kandidatstuderende Tonghan Gu (til højre) arbejder med teknikere på en facilitet i Vasai, Indien, at producere et parti brugsklare terapeutiske fødevarer i pulverform. Formlen, han har udviklet, b -
 Nu kan metaloverflader være øjeblikkelige bakteriedræbereEn laser forbereder sig på at teksturere overfladen af kobber, forbedrer dets antimikrobielle egenskaber. Kredit:Purdue University /Kayla Wiles Bakterielle patogener kan leve på overflader i fle
Nu kan metaloverflader være øjeblikkelige bakteriedræbereEn laser forbereder sig på at teksturere overfladen af kobber, forbedrer dets antimikrobielle egenskaber. Kredit:Purdue University /Kayla Wiles Bakterielle patogener kan leve på overflader i fle -
 En ny måde at pakke flydende dråber på kan forbedre medicinafgivelsenKredit:CC0 Public Domain Forskere har udviklet en hurtigere, billigere måde at belægge flydende medicin på, en opfindelse, der kunne forbedre, hvordan lægemidler afgives i kroppen. Den nye indkap
En ny måde at pakke flydende dråber på kan forbedre medicinafgivelsenKredit:CC0 Public Domain Forskere har udviklet en hurtigere, billigere måde at belægge flydende medicin på, en opfindelse, der kunne forbedre, hvordan lægemidler afgives i kroppen. Den nye indkap -
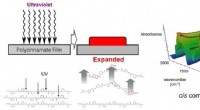 Fotoudvidelse:Biobaserede polyestere hård filmDen UV-inducerede deformation af polycinnamatet blev analyseret ved tidsopløst IR-spektroskopi, og det blev bekræftet, at fotoudvidelse fandt sted baseret på trans-til-cis-isomerisering af cinnamatenh
Fotoudvidelse:Biobaserede polyestere hård filmDen UV-inducerede deformation af polycinnamatet blev analyseret ved tidsopløst IR-spektroskopi, og det blev bekræftet, at fotoudvidelse fandt sted baseret på trans-til-cis-isomerisering af cinnamatenh
- Hvad holder solen sammen under nuklear reaktion?
- Hvilken tilstand af stof indeholder de mest energiske partikler?
- Hvordan indfødt viden fremmer moderne videnskab og teknologi
- Kunne vi ændre den aksiale hældning?
- Hvilken videnskabelig metode følger eksperimentet?
- Hvad produceres i energitransformation?


