Ionledningsevne af NaCl:faste vs. smeltede tilstande forklaret
1. NaCls ioniske natur:
* Natriumchlorid (NaCl) er en ionisk forbindelse. Det betyder, at det er dannet af den elektrostatiske tiltrækning mellem positivt ladede natriumioner (Na+) og negativt ladede chloridioner (Cl-).
2. Solid State:
* I fast tilstand er disse ioner låst i et stift, krystallinsk gitter. Ionerne er tæt pakket og holdt på plads af stærke elektrostatiske kræfter. Denne stive struktur forhindrer den frie bevægelse af ioner.
* Uden frit bevægelige ladningsbærere (som ioner) kan elektricitet ikke flyde. Derfor er fast NaCl en dårlig leder af elektricitet.
3. Smeltet tilstand:
* Når NaCl smelter, bryder ionerne fri fra deres faste positioner. De stærke elektrostatiske kræfter, der holder ionerne sammen, svækkes, så de kan bevæge sig mere frit.
* Disse mobile ioner fungerer som ladningsbærere. Når en spænding påføres, bevæger de positive natriumioner sig mod den negative elektrode, og de negative kloridioner bevæger sig mod den positive elektrode. Denne strøm af ioner udgør en elektrisk strøm.
Opsummering:
* Fast NaCl: Ioner er faste, ingen gratis ladningsbærere, ingen ledningsevne.
* Smeltet NaCl: Ioner er mobile, gratis ladningsbærere, god ledningsevne.
 Varme artikler
Varme artikler
-
 Bæredygtig, stærkt selektiv biokatalytisk omdannelse af aldehyder til carboxylsyrerForsidebillede af den aktuelle udgave af Green Chemistry med HIMS/Biocat -forskningen. Forskere fra University of Amsterdams Vant Hoff Institute for Molecular Sciences (HIMS) har udviklet den førs
Bæredygtig, stærkt selektiv biokatalytisk omdannelse af aldehyder til carboxylsyrerForsidebillede af den aktuelle udgave af Green Chemistry med HIMS/Biocat -forskningen. Forskere fra University of Amsterdams Vant Hoff Institute for Molecular Sciences (HIMS) har udviklet den førs -
 Forståelse af ustabile atomer:ioner, radioaktivitet og atomisk stabilitetAf Chris Deziel, Opdateret 24. marts 2022 kotoffei/iStock/GettyImages TL;DR (for lang; læste ikke) Ioner er elektrisk ustabile og danner hurtigt kemiske bindinger. Atomer med ubalancerede kerner uds
Forståelse af ustabile atomer:ioner, radioaktivitet og atomisk stabilitetAf Chris Deziel, Opdateret 24. marts 2022 kotoffei/iStock/GettyImages TL;DR (for lang; læste ikke) Ioner er elektrisk ustabile og danner hurtigt kemiske bindinger. Atomer med ubalancerede kerner uds -
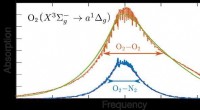 Forskere opdager, hvordan kolliderende iltmolekyler absorberer lysFigur:Eksperimentelle og teoretiske spektre for lysabsorption på grund af kollision af ilt (O2) molekyler med andre iltmolekyler og med nitrogen (N2) molekyler. Som vist her, absorptionen på grund af
Forskere opdager, hvordan kolliderende iltmolekyler absorberer lysFigur:Eksperimentelle og teoretiske spektre for lysabsorption på grund af kollision af ilt (O2) molekyler med andre iltmolekyler og med nitrogen (N2) molekyler. Som vist her, absorptionen på grund af -
 Forbehandling af gener grønne alger med lud, urinstof øger bakteriel produktion af biogasI kontrolbilledet (til venstre), underlaget er glat og intakt, men på billedet efter forbehandling af NaOH-urinstof (højre), underlaget nedbrydes. Kredit:Harbin Engineering University I mere end 6
Forbehandling af gener grønne alger med lud, urinstof øger bakteriel produktion af biogasI kontrolbilledet (til venstre), underlaget er glat og intakt, men på billedet efter forbehandling af NaOH-urinstof (højre), underlaget nedbrydes. Kredit:Harbin Engineering University I mere end 6
- 2 eksempler på anvendte kræfter forårsager ændring i formobjektet?
- Hvordan forårsager solen fordampning?
- Kraftige stratosfæriske vinde målt på Jupiter for første gang
- Satellit ser Atlantic Tropical Depression 14 former ud for Afrikas vestkyst
- Hvad er kirtlen i hjernen, der reguleres af lys?
- Hvad er den videnskabelige undersøgelse af strukturen, hvis jorden?


