Opløselighed af salt:Hvorfor opløses i vand, ikke olie?
Forstå polaritet
* Vand (H₂O) er et polært molekyle: Det betyder, at den har en let positiv ende (brintatomerne) og en lidt negativ ende (iltatomet). Denne ujævne fordeling af ladningen skaber en "dipol".
* Olie er et ikke-polært molekyle: Dens molekyler har en jævn fordeling af ladning uden tydelige positive eller negative ender.
* Salt (NaCl) er en ionisk forbindelse: Den består af positivt ladede natriumioner (Na+) og negativt ladede chloridioner (Cl-) holdt sammen af elektrostatisk tiltrækning.
Opløsning af salt
* Vands polaritet er nøglen: Vandmolekyler omgiver saltionerne, med den negative iltende af vandmolekylerne tiltrukket af de positive natriumioner, og den positive brintende af vandmolekylerne tiltrukket af de negative chloridioner.
* At bryde bindingerne: Denne tiltrækning overvinder ionbindingen, der holder saltet sammen, hvilket får saltet til at opløses. Saltionerne bliver omgivet af vandmolekyler og spredes gennem opløsningen.
Hvorfor salt ikke opløses i olie
* Mangel på tiltrækning: Olie, som er upolær, har ikke den samme ladningsadskillelse som vand. Det kan ikke effektivt omgive og tiltrække de ladede saltioner.
* Ingen bindingsbrud: Da der ikke er nogen stærk tiltrækning mellem oliemolekylerne og saltionerne, forbliver de ioniske bindinger, der holder saltet sammen, intakte.
Kort sagt: Forestil dig saltioner som magneter. Vand er som en flok små magneter med modsatte poler, der trækker saltionerne fra hinanden. Olie er som en flok ikke-magnetiske kugler; der er ingen tiltrækning til at trække saltionerne fra hinanden.
 Varme artikler
Varme artikler
-
 Videnskabsprojekter:Fryser sukkervand hurtigere end rent vand?Af Jack Brubaker Opdateret 30. august 2022 Statslige og kommunale myndigheder spreder ofte salt på vejene for at holde dem sikre. Ved at sænke isens smeltepunkt - en effekt kendt som frysepunktsdepr
Videnskabsprojekter:Fryser sukkervand hurtigere end rent vand?Af Jack Brubaker Opdateret 30. august 2022 Statslige og kommunale myndigheder spreder ofte salt på vejene for at holde dem sikre. Ved at sænke isens smeltepunkt - en effekt kendt som frysepunktsdepr -
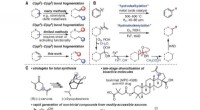 En mere effektiv måde at spalte vedhængende olefiner fra terpener og lignende forbindelserKoncept og anvendelser af hydrodealkenylativ fragmentering af C(sp 3 )–C(sp 2 ) obligationer. (A) Dekonstruktiv fragmentering af C-C-bindinger. (B) Oversigt og foreslået mekanisme for hydrodealken
En mere effektiv måde at spalte vedhængende olefiner fra terpener og lignende forbindelserKoncept og anvendelser af hydrodealkenylativ fragmentering af C(sp 3 )–C(sp 2 ) obligationer. (A) Dekonstruktiv fragmentering af C-C-bindinger. (B) Oversigt og foreslået mekanisme for hydrodealken -
 Hvordan Jorden fanger solenergi:Videnskaben om planetarisk opvarmningAf David Sarokin Opdateret 24. marts 2022 Design Pics/Carl Shaneff/Design Pics/Getty Images Solen udstråler energi i alle retninger. Det meste af det spreder sig ud i rummet, men den lille del af s
Hvordan Jorden fanger solenergi:Videnskaben om planetarisk opvarmningAf David Sarokin Opdateret 24. marts 2022 Design Pics/Carl Shaneff/Design Pics/Getty Images Solen udstråler energi i alle retninger. Det meste af det spreder sig ud i rummet, men den lille del af s -
 Forskere skaber ny aluminiumslegering med fleksibilitet, styrke, lethedDetaljer lavet af Al-Ni-La kompositmateriale Kredit:© Sergey Gnuskov/NUST MISIS Aluminium er et af de mest lovende materialer til luftfarts- og bilindustrien. Forskere fra National University of S
Forskere skaber ny aluminiumslegering med fleksibilitet, styrke, lethedDetaljer lavet af Al-Ni-La kompositmateriale Kredit:© Sergey Gnuskov/NUST MISIS Aluminium er et af de mest lovende materialer til luftfarts- og bilindustrien. Forskere fra National University of S
- Typer af akvatiske planter og dyr i Mississippi-floden
- Hvilke skridt kan du tage for at opløse et opløst stof i løsningen den korteste tid?
- Sådan finder du drejepoint af en polynom
- Sådan fungerer Mælkevejen
- Undersøgelse undersøger dielektrisk keramik med lav permittivitet til mikrobølge/millimeterbølge…
- Hvad opstår, når tyngdekraften af sol og måne fungerer mod hinanden for at skabe et lille dagli…


