Videnskabsprojekter:Fryser sukkervand hurtigere end rent vand?
Af Jack Brubaker
Opdateret 30. august 2022
Statslige og kommunale myndigheder spreder ofte salt på vejene for at holde dem sikre. Ved at sænke isens smeltepunkt - en effekt kendt som frysepunktsdepression - hjælper salt med at holde trafikken flydende. Det samme princip giver et sjovt og lærerigt videnskabeligt eksperiment, der kan spænde fra en hurtig demonstration til et detaljeret projekt komplet med matematiske forudsigelser. Alt du behøver er en gryde og et termometer.
Frysepunktsdepression
Når et fast stof opløses i vand, bryder det i små partikler. For sukker er disse individuelle molekyler; for salte såsom natriumchlorid er de ladede ioner. Disse partikler forstyrrer vandmolekylers evne til at arrangere til et fast stof, når temperaturen nærmer sig frysepunktet, og sænker dermed frysepunktet. Dette fænomen er universelt på tværs af væsker, ikke kun vand.
Måling af frysning
At vælge den rigtige måling er nøglen. I stedet for at spørge, hvilken prøve fryser først, skal du fokusere på den temperatur, ved hvilken hver opløsning når fast tilstand. Denne tilgang afslører, hvordan urenheder ændrer frysepunktet og giver et klarere, mere videnskabeligt meningsfuldt resultat.
Bliv matematisk
Den etablerede ligning for frysepunktsdepression er:
ΔT=–k·m
hvor er opløsningsmidlets molale frysepunktsdepressionskonstant og er opløsningens molalitet (mol partikler pr. kilogram opløsningsmiddel). For vand svarer til 1,86°C·kgmol⁻¹. Saccharose (C₁₂H₂2O11) har en molekylvægt på 342,3 gmol⁻¹, så formlen forenkler til:
ΔT=–1,86×(gram saccharose/342,3/kg vand)
Eksempel:Opløs 10 g saccharose i 100 ml (≈0,100 kg) vand. ΔT=–1,86×(10/342,3/0,1)≈–0,54°C. Således fryser opløsningen ved ca. 0,54°C under rent vands frysepunkt.
Avancerede projekter
Ved at omarrangere formlen kan eleverne bestemme et opløst stofs molekylvægt eksperimentelt:
MW=(–1,86×gram saccharose)/(ΔT×kg vand)
Mange high-school og college kemi kurser bruger denne metode til at finde molekylvægten af ukendte stoffer. En lignende tilgang fungerer for kogepunktsundersøgelser, hvor konstanten ændres til 0,52.
 Varme artikler
Varme artikler
-
 Synligt lys og nanopartikelkatalysatorer producerer ønskelige bioaktive molekylerMolekyler adsorberer på overfladen af halvledernanopartikler i meget specifikke geometrier. Nanopartiklerne bruger energi fra indfaldende lys til at aktivere molekylerne og smelte dem sammen til at
Synligt lys og nanopartikelkatalysatorer producerer ønskelige bioaktive molekylerMolekyler adsorberer på overfladen af halvledernanopartikler i meget specifikke geometrier. Nanopartiklerne bruger energi fra indfaldende lys til at aktivere molekylerne og smelte dem sammen til at -
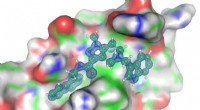 Ny terapeutisk strategi mod sovesygeStruktur af grænsefladen mellem PEX14 og PEX5 (bagpå) inklusive strukturen af inhibitoren (foran). Kredit:Dr. Grzegorz Popowicz, Helmholtz Zentrum München Et nyudviklet lille molekyle dræber sel
Ny terapeutisk strategi mod sovesygeStruktur af grænsefladen mellem PEX14 og PEX5 (bagpå) inklusive strukturen af inhibitoren (foran). Kredit:Dr. Grzegorz Popowicz, Helmholtz Zentrum München Et nyudviklet lille molekyle dræber sel -
 Kemikere udvikler en ny teknologi til at forhindre lithium-ion-batterier i at antændeGasserne byggede sig op og fik det ikke-beskyttede batteri (til venstre) til at svulme op. Det kan føre til en eksplosion. Det beskyttede batteri (til højre) forbliver fladt, da det beskyttende lag bl
Kemikere udvikler en ny teknologi til at forhindre lithium-ion-batterier i at antændeGasserne byggede sig op og fik det ikke-beskyttede batteri (til venstre) til at svulme op. Det kan føre til en eksplosion. Det beskyttede batteri (til højre) forbliver fladt, da det beskyttende lag bl -
 Kemikere lærer at opdage phenoler i røget madprøver ved hjælp af vitamin B4Påvisning af phenoler i pølse ved hjælp af vitamin B4 Kredit:SPbU I dag, phenoler bruges til at producere medicin, maling, og billige møbler af spånplader eller MDF -paneler og også til forarbejdn
Kemikere lærer at opdage phenoler i røget madprøver ved hjælp af vitamin B4Påvisning af phenoler i pølse ved hjælp af vitamin B4 Kredit:SPbU I dag, phenoler bruges til at producere medicin, maling, og billige møbler af spånplader eller MDF -paneler og også til forarbejdn
- Gammel, firbenet hval med odderlignende træk fundet langs Perus kyst
- Florida Tarantulaer og andre edderkopper
- Ny lysteknik kan resultere i mindre påtrængende, mere effektiv diagnose for patienter
- Kvantificeret i stor skala:Underliggende drivkræfter for underliggende biomasse og dens allokering
- Plantestruktur, der opbevarer mad og pigmenter?
- Hvor mange amerikanske astronauter har udforsket månen?


