Forståelse af CO3^2-:Kovalente vs. ioniske bindinger forklaret
* ioniske bindinger: Ionbindinger dannes mellem et metal og et ikke-metal. Metalatomet mister elektroner for at blive en positivt ladet kation, mens ikke-metalatomet får elektroner til at blive en negativt ladet anion. Disse modsat ladede ioner tiltrækkes af hinanden og danner ionbindingen.
* Karbonationstruktur:
* Kulstof (C) er et ikke-metal.
* Ilt (O) er et ikke-metal.
* Carbonationen (CO3^2-) dannes, når kulstof deler elektroner med tre oxygenatomer.
Men bindingerne i carbonation er faktisk en blanding af ionisk og kovalent karakter.
* Kovalent karakter: Kulstof og ilt deler elektroner på en kovalent måde for at danne bindingerne i carbonationen. Men på grund af iltens høje elektronegativitet bruger de delte elektroner mere tid omkring iltatomerne, hvilket skaber en delvis negativ ladning på iltatomerne og en delvis positiv ladning på carbonatomet.
* ionisk karakter: Denne ujævne fordeling af elektroner fører til en samlet negativ ladning på karbonationen, hvilket gør den til en anion.
Opsummering:
* Carbonationen holdes sammen af kovalente bindinger i selve ionen.
* Carbonationen som helhed danner ioniske bindinger med andre positivt ladede ioner i en forbindelse.
Sig til, hvis du har andre kemispørgsmål!
 Varme artikler
Varme artikler
-
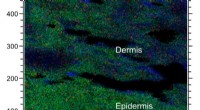 Ny metode kortlægger kemikalier i huden3-D billeddannelse af en hudsektion, hvor nikkelindholdet måles. Det røde område repræsenterer tilstedeværelsen af nikkel. Kredit:Per Malmberg En ny metode til at undersøge huden kan reducere an
Ny metode kortlægger kemikalier i huden3-D billeddannelse af en hudsektion, hvor nikkelindholdet måles. Det røde område repræsenterer tilstedeværelsen af nikkel. Kredit:Per Malmberg En ny metode til at undersøge huden kan reducere an -
 Forskere udvider mulighederne for PET -billeddannelse gennem enklere kemiKredit:CC0 Public Domain Forskere ved University of Arizona har udviklet en hurtig, forenklet metode til fremstilling af radiomærkningsforbindelser, der anvendes til positronemissionstomografi, og
Forskere udvider mulighederne for PET -billeddannelse gennem enklere kemiKredit:CC0 Public Domain Forskere ved University of Arizona har udviklet en hurtig, forenklet metode til fremstilling af radiomærkningsforbindelser, der anvendes til positronemissionstomografi, og -
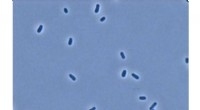 CO2 som råstof til plast og andre produkterLysmikrofotografi af celler af den gramnegative bakterie-Methylorubrum extor-quens AM1. Kredit:Fraunhofer-Gesellschaft Kuldioxid er en af de vigtigste drivkræfter bag klimaændringer - hvilket be
CO2 som råstof til plast og andre produkterLysmikrofotografi af celler af den gramnegative bakterie-Methylorubrum extor-quens AM1. Kredit:Fraunhofer-Gesellschaft Kuldioxid er en af de vigtigste drivkræfter bag klimaændringer - hvilket be -
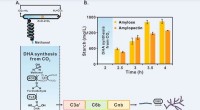 Kinesiske videnskabsmænd rapporterer om stivelsesyntese fra kuldioxidStivelsessyntese via kunstig stivelse anabolsk vej (ASAP) fra kuldioxid. Kredit:TIBCAS Kinesiske videnskabsmænd rapporterede for nylig om en de novo-rute til kunstig stivelsessyntese fra kuldioxid
Kinesiske videnskabsmænd rapporterer om stivelsesyntese fra kuldioxidStivelsessyntese via kunstig stivelse anabolsk vej (ASAP) fra kuldioxid. Kredit:TIBCAS Kinesiske videnskabsmænd rapporterede for nylig om en de novo-rute til kunstig stivelsessyntese fra kuldioxid
- Hvorfor Jorden skælver:Et nærmere kig på, hvad der foregår under jorden
- Hvordan indstiller du uret på Eclipse Unit?
- Blandet tidevand forklaret:Hvordan ulige høje og lave bølger former globale kyster
- Hvilken træning gjorde Neil Armstrong for at være en astronat?
- Hvilken slags energi har en helikopter?
- En base er et stof, der danner hydrogenioner i vandopløsning?


