Ilt vs. Xenonioniseringsenergier:En sammenlignende analyse
Her er hvorfor:
* Elektronkonfiguration: Oxygen har elektronkonfigurationen 1s²2s²2p⁴, mens xenon har konfigurationen [Kr]4d¹⁰5s²5p⁶. Det betyder, at de yderste elektroner i ilt er i 2p subshell, mens de yderste elektroner i xenon er i 5p subshell.
* Afskærmningseffekt: 5p-elektronerne i xenon er meget længere fra kernen end 2p-elektronerne i oxygen. De oplever en større afskærmningseffekt fra de indre elektroner, hvilket reducerer tiltrækningen mellem kernen og de yderste elektroner.
* Atomladning: Xenon har en meget større nuklear ladning end oxygen på grund af dets større antal protoner. Dette øger tiltrækningen mellem kernen og dens elektroner.
Men den større nukleare ladning i xenon er ikke nok til at overvinde afskærmningseffekten og den større afstand af 5p-elektronerne. Dette resulterer i en betydeligt lavere ioniseringsenergi for xenon sammenlignet med oxygen .
Opsummering:
* Oxygen har en højere ioniseringsenergi end xenon.
* Denne forskel skyldes kombinationen af afskærmningseffekter, afstand fra kernen og nuklear ladning.
 Varme artikler
Varme artikler
-
 Hvilke drikkevarer sprænger med umami-potentiale?Kredit:Pixabay/CC0 Public Domain En femte grundsmag er sneget sig ind i vores konceptualisering af fødevarer i de seneste år - umami. på japansk, umami kan groft sagt oversættes til smagfuld lække
Hvilke drikkevarer sprænger med umami-potentiale?Kredit:Pixabay/CC0 Public Domain En femte grundsmag er sneget sig ind i vores konceptualisering af fødevarer i de seneste år - umami. på japansk, umami kan groft sagt oversættes til smagfuld lække -
 Ny teknik til at forbedre duktiliteten af keramiske materialer til missiler, motorerPurdue University-forskere har udviklet en ny proces for at hjælpe med at overvinde keramiks skøre natur og gøre den mere holdbar. Kredit:Purdue University/Chris Adam Noget så simpelt som et elekt
Ny teknik til at forbedre duktiliteten af keramiske materialer til missiler, motorerPurdue University-forskere har udviklet en ny proces for at hjælpe med at overvinde keramiks skøre natur og gøre den mere holdbar. Kredit:Purdue University/Chris Adam Noget så simpelt som et elekt -
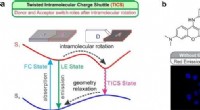 Forskere opdager ny ladningsoverførsel og adskillelsesproces(a) Skematisk illustration af de twisted intramolecular charge shuttle (TICS) mekanismer; D og A betegner elektrondonerende og elektronaccepterende fragmenter, henholdsvis. (b) Reaktionsmekanisme for
Forskere opdager ny ladningsoverførsel og adskillelsesproces(a) Skematisk illustration af de twisted intramolecular charge shuttle (TICS) mekanismer; D og A betegner elektrondonerende og elektronaccepterende fragmenter, henholdsvis. (b) Reaktionsmekanisme for -
 Ny katalysator til brintproduktion er et skridt mod rent brændstofForsiden viser produktionen af brintgas, når elektroner og protoner mødes på ruthenium-ion-komplekserede grafitiske carbonnitrid-nanoark understøttet på grafenoverfladen. Billedet er baseret på en g
Ny katalysator til brintproduktion er et skridt mod rent brændstofForsiden viser produktionen af brintgas, når elektroner og protoner mødes på ruthenium-ion-komplekserede grafitiske carbonnitrid-nanoark understøttet på grafenoverfladen. Billedet er baseret på en g


