Beregning af opløsningsvolumen til neutralisering:En trin-for-trin guide
1. Skriv den afbalancerede kemiske ligning:
HCl (aq) + KOH (aq) → KCl (aq) + H2O (l)
2. Bestem molerne af kaliumhydroxid (KOH):
* Konverter volumen af KOH-opløsning fra milliliter til liter:24,3 mL * (1 L / 1000 mL) =0,0243 L
* Multiplicer volumenet af KOH-opløsning med dens molaritet:0,0243 L * 0,200 mol/L =0,00486 mol KOH
3. Brug molforholdet fra den balancerede ligning til at finde mol saltsyre (HCl):
* Den afbalancerede ligning viser et molforhold på 1:1 mellem HCl og KOH. Derfor vil 0,00486 mol KOH reagere med 0,00486 mol HCl.
4. Beregn volumen af HCl-opløsning:
* Divider mol HCl med molariteten af HCl-opløsningen:0,00486 mol / 0,357 mol/L =0,0136 L
* Konverter volumen fra liter til milliliter:0,0136 L * (1000 mL / 1 L) =13,6 mL
Svar: Du skal bruge 13,6 mL af den 0,357 M saltsyreopløsning for at neutralisere 24,3 ml af den 0,200 M kaliumhydroxidopløsning.
 Varme artikler
Varme artikler
-
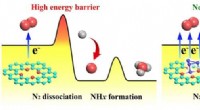 Opnåelse af højeffektiv ammoniaksyntese ved at ændre det hastighedsbestemmende trinSkematisk illustration af ændring af det hastighedsbestemmende trin i nitrogenreduktionsreaktionen ved at indføre kobolt-enkeltklynge i katalysatoren. Den cyan, rød, lilla, og grå kugler repræsenterer
Opnåelse af højeffektiv ammoniaksyntese ved at ændre det hastighedsbestemmende trinSkematisk illustration af ændring af det hastighedsbestemmende trin i nitrogenreduktionsreaktionen ved at indføre kobolt-enkeltklynge i katalysatoren. Den cyan, rød, lilla, og grå kugler repræsenterer -
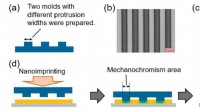 Forskning afslører kvantitative og højopløselige trykfunktioner af trykfølsomt materiale(a) Tværsnitsbillede af to siliciumforme. (b) Fotografier af en storskala siliciumform. (c) AFM billede af en smal skala silicium form. (d) Illustration til undersøgelse af rumlig opløsning ved hjælp
Forskning afslører kvantitative og højopløselige trykfunktioner af trykfølsomt materiale(a) Tværsnitsbillede af to siliciumforme. (b) Fotografier af en storskala siliciumform. (c) AFM billede af en smal skala silicium form. (d) Illustration til undersøgelse af rumlig opløsning ved hjælp -
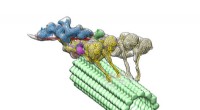 Mikroskopiske vogne leverer molekyler i vores cellerDynein-dynactin-komplekset (flerfarvet) driver ned i en mikrotubuli (grøn). De fire motordomæner er vist med gult. Dynactin (blå) udgør stilladset for at holde de to dyneiner sammen. Kredit:Danielle G
Mikroskopiske vogne leverer molekyler i vores cellerDynein-dynactin-komplekset (flerfarvet) driver ned i en mikrotubuli (grøn). De fire motordomæner er vist med gult. Dynactin (blå) udgør stilladset for at holde de to dyneiner sammen. Kredit:Danielle G -
 Ny, meget stabil katalysator kan hjælpe med at omdanne vand til brændstofPostdoktor Jaemin Kim, professor i kemisk og biomolekylær teknik Hong Yang og kandidatstuderende Pei-Chieh (Jack) Shih er en del af et team, der udviklede et nyt materiale, der hjælper med at spalte v
Ny, meget stabil katalysator kan hjælpe med at omdanne vand til brændstofPostdoktor Jaemin Kim, professor i kemisk og biomolekylær teknik Hong Yang og kandidatstuderende Pei-Chieh (Jack) Shih er en del af et team, der udviklede et nyt materiale, der hjælper med at spalte v
- Hvilken type bundkort bruger en energibesparende monitor?
- Neuroner, hvilke er indpakket i en fed membran er?
- Hvad kan et grønt forår betyde for ildtiden?
- Første vellykkede laserindfangning af cirkulære Rydberg -atomer
- Grækenlands første undervandsmuseum åbner den antikke verden for dykkerturister
- Ramme til at spore individuelle kulstofatomers vej


