Frysepunktsdepression:Hvordan salt sænker frysetemperaturerne
* Afbrydelse af vandmolekyler: Når salt opløses i vand, forstyrrer saltionerne (natrium og chlorid) den normale hydrogenbinding mellem vandmolekyler. Dette gør det sværere for vandmolekyler at danne den krystallinske struktur, der kræves til frysning.
* Sænkning af damptrykket: De opløste saltioner sænker også vandets damptryk, hvilket gør det sværere for vandet at fordampe. Det betyder, at vandet skal være koldere for at nå frysepunktet.
Faktorer, der påvirker frysepunktsdepression:
* Salttype: Forskellige salte har forskellige frysepunktssænkningsværdier. For eksempel er calciumchlorid mere effektivt til at sænke frysepunktet end natriumchlorid.
* Saltkoncentration: Jo mere salt du tilsætter, jo lavere bliver frysepunktet.
* Væsketype: Frysepunktsnedsættelsen påvirkes også af væsketypen. Salt vil fx have en større effekt på vands frysepunkt end på alkoholens frysepunkt.
Applikationer:
* Vejsalt: Salt bruges til at afise veje om vinteren, fordi det sænker vandets frysepunkt og forhindrer is i at dannes.
* Fødevarekonservering: Salt bruges til konservering af fødevarer, fordi det sænker frysepunktet for vand i maden, hvilket gør det sværere for bakterier at vokse.
Vigtig bemærkning: Mens salt sænker frysepunktet for vand, eliminerer det det ikke helt. Der er en grænse for, hvor meget frysepunktet kan sænkes.
 Varme artikler
Varme artikler
-
 Borat bioaktivt glas i nanoskala:Et næste generations materiale til hudhelingBorat bioaktivt glas i nanoskala. Kredit:MA Kun For nylig, ved hjælp af en steady-state stærk magnetfelt eksperimentel enhed, forskere konstruerede bioaktivt boratglas i nanoskala (Nano-HCA@BG), s
Borat bioaktivt glas i nanoskala:Et næste generations materiale til hudhelingBorat bioaktivt glas i nanoskala. Kredit:MA Kun For nylig, ved hjælp af en steady-state stærk magnetfelt eksperimentel enhed, forskere konstruerede bioaktivt boratglas i nanoskala (Nano-HCA@BG), s -
 Lys på effektivitetstab i organiske solcellerVed hjælp af en kompleks laseropsætning, holdet opdagede, at i modsætning til de seneste rapporter, betydelige ioniseringsenergiforskydninger var nødvendige for at generere ladninger. Kredit:© 2020 KA
Lys på effektivitetstab i organiske solcellerVed hjælp af en kompleks laseropsætning, holdet opdagede, at i modsætning til de seneste rapporter, betydelige ioniseringsenergiforskydninger var nødvendige for at generere ladninger. Kredit:© 2020 KA -
 Nyt lavprismateriale til belysning og diagnostik producerer hvidt lys, der imiterer sollysHackmanitten udviklet af forskerne. Kredit:Universitetet i Turku Forskere ved Universitetet i Turku, Finland, har udviklet et syntetisk materiale baseret på det naturlige hackmanitmineral, som pro
Nyt lavprismateriale til belysning og diagnostik producerer hvidt lys, der imiterer sollysHackmanitten udviklet af forskerne. Kredit:Universitetet i Turku Forskere ved Universitetet i Turku, Finland, har udviklet et syntetisk materiale baseret på det naturlige hackmanitmineral, som pro -
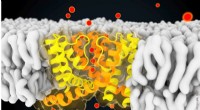 Strukturelle og dynamiske forskelle mellem selektive og ikke-selektive ionkanalerSnapshot taget under computersimuleringen af NaK-kanalen - Denne kanal (vist i gult og orange) muliggør strømmen af ioner (f.eks. kaliumioner [røde kugler]) over cellemembranen. (Membranlipiderne
Strukturelle og dynamiske forskelle mellem selektive og ikke-selektive ionkanalerSnapshot taget under computersimuleringen af NaK-kanalen - Denne kanal (vist i gult og orange) muliggør strømmen af ioner (f.eks. kaliumioner [røde kugler]) over cellemembranen. (Membranlipiderne
- Hvad er to egenskaber ved en ideel gas, der ikke sandt er en rigtig gas?
- Hypertoniske løsninger:definition, egenskaber og celleeffekter
- Økologiske TFT'er, der udviser bandlignende transport
- Forståelse af elektrisk strøm:Frie elektroners rolle
- Vand spiller en vigtig rolle i at skulpturere landskabet på kontinenter, fordi?
- Hvem opdagede først promethium?


