p-Nitrophenol-farveændringer:sure vs. basisløsninger forklaret
Forståelse af kemien
* p-Nitrophenol er en svag syre. I sin neutrale form eksisterer det som et bleggult fast stof.
* I sure opløsninger , forbliver forbindelsen i sin neutrale form (p-nitrophenol) og bevarer sin lysegule farve.
* I grundlæggende løsninger , mister p-nitrophenol en proton fra sin hydroxylgruppe (-OH) og danner p-nitrophenoxidionen , som er intenst gul.
Farveændringer:
* Surt medium: Bleg gul
* Grundlæggende medium: Intens gul
Forklaring af farveændringen
Farveændringen skyldes ændringen i molekylets elektroniske struktur.
1. Neutral form: Den neutrale form af p-nitrophenol har et udvidet pi-elektronsystem på grund af konjugation mellem nitrogruppen (-NO2) og den aromatiske ring. Denne konjugation muliggør absorption af lys i det ultraviolette område, hvilket resulterer i en bleggul farve.
2. p-Nitrophenoxid-ion: Når p-nitrophenol mister en proton, danner den p-nitrophenoxid-ionen. Den negative ladning på oxygenatomet udvider pi-elektronsystemet yderligere, hvilket øger konjugationen. Denne øgede konjugation flytter absorptionen af lys til længere bølgelængder, bevæger sig ind i det synlige område og resulterer i en intens gul farve.
Opsummering:
Farveændringen af p-nitrophenol fra bleggul til intens gul ved at gå fra sure til basiske medier skyldes dannelsen af p-nitrophenoxid-ionen, som har et mere udvidet pi-elektronsystem og absorberer lys i det synlige område.
 Varme artikler
Varme artikler
-
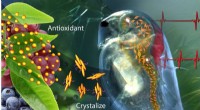 Smart antioxidantholdig polymer reagerer på kroppens kemi, miljøEt nyt lægemiddelleveringssystem, der indeholder krystalliseret catechin - en antioxidant, der findes i grøn te og frugt - kan mærke problemer og reagere ved at frigive antioxidant for at genoprette e
Smart antioxidantholdig polymer reagerer på kroppens kemi, miljøEt nyt lægemiddelleveringssystem, der indeholder krystalliseret catechin - en antioxidant, der findes i grøn te og frugt - kan mærke problemer og reagere ved at frigive antioxidant for at genoprette e -
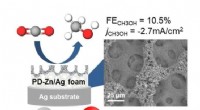 Omdannelse af kuldioxid til methanol(Venstre) Skematisk fremstilling af methanol ved elektrokatalytisk reduktion af kuldioxid ved brug af PD-Zn/Ag skumkatalysatoren. (Højre) Scanning elektronmikroskopi billede af overfladen af PD-Zn/A
Omdannelse af kuldioxid til methanol(Venstre) Skematisk fremstilling af methanol ved elektrokatalytisk reduktion af kuldioxid ved brug af PD-Zn/Ag skumkatalysatoren. (Højre) Scanning elektronmikroskopi billede af overfladen af PD-Zn/A -
 Revolutionære billeder af krystallers fødselForskerne brugte lasere til at afsløre den molekylære struktur på arbejde under kernedannelse, men også til at fremkalde kernedannelse og observere dets spektrale fingeraftryk. Kredit:© Oscar Urquidi
Revolutionære billeder af krystallers fødselForskerne brugte lasere til at afsløre den molekylære struktur på arbejde under kernedannelse, men også til at fremkalde kernedannelse og observere dets spektrale fingeraftryk. Kredit:© Oscar Urquidi -
 Bioprinting af komplekst levende væv på få sekunderDen hule muse-lungearteriemodel. Kredit:Alain Herzog/2019 EPFL Vævsingeniører skaber kunstige organer og væv, der kan bruges til at udvikle og teste nye lægemidler, reparere beskadiget væv og endd
Bioprinting af komplekst levende væv på få sekunderDen hule muse-lungearteriemodel. Kredit:Alain Herzog/2019 EPFL Vævsingeniører skaber kunstige organer og væv, der kan bruges til at udvikle og teste nye lægemidler, reparere beskadiget væv og endd


