Benzenstruktur:En omfattende guide til molekylær binding
Grundlæggende struktur:
* Seks-medlemsring: Benzen består af en ring med seks carbonatomer, der hver er bundet til et brintatom.
* Dobbeltobligationer: Den klassiske fremstilling viser skiftevis enkelt- og dobbeltbindinger mellem carbonatomerne. Dette giver udseendet af en "Kekule-struktur".
Virkeligheden er mere kompleks:
* Delokaliserede elektroner: Elektronerne i dobbeltbindingerne er ikke fikseret mellem specifikke kulstofatomer. I stedet delokaliseres de og fordeles jævnt rundt i hele ringen. Dette skaber en "pi elektronsky" over og under ringens plan.
* Resonanshybrid: Den faktiske struktur af benzen er en resonanshybrid, hvilket betyder, at det er en kombination af flere mulige strukturer. Kekule-strukturen er kun én bidragende form.
Hvorfor er dette vigtigt?
* Stabilitet: Delokaliseringen af elektroner giver benzen enestående stabilitet. Det gennemgår ikke let typiske alkenreaktioner som addition.
* Reaktivitet: På trods af dets stabilitet kan benzen undergå andre reaktioner, primært elektrofile aromatiske substitutionsreaktioner, som er vigtige i organisk kemi.
Repræsentationer:
* Kekule-struktur: Dette er den klassiske repræsentation med skiftende enkelt- og dobbeltbindinger.
* Cirkel i en sekskant: Dette er en mere moderne og forenklet fremstilling. Cirklen repræsenterer den delokaliserede pi-elektronsky.
Lad mig vide, hvis du gerne vil dykke ned i specifikke aspekter af benzens struktur, dets egenskaber eller dets reaktioner!
 Varme artikler
Varme artikler
-
 Ny opdagelse hjælper myndighederne med at identificere heroinets oprindelseFIU kemi Ph.D. studerende Joshua DeBord analyserer en heroinprøve ved hjælp af udstyr på University of Miami. Kredit:Florida International University Forskere ved Florida International Universitys
Ny opdagelse hjælper myndighederne med at identificere heroinets oprindelseFIU kemi Ph.D. studerende Joshua DeBord analyserer en heroinprøve ved hjælp af udstyr på University of Miami. Kredit:Florida International University Forskere ved Florida International Universitys -
 Ingeniører demonstrerer superstærk, vendbart klæbemiddel, der fungerer som snegleslime (opdaterin…Snegle kan forankre sig på plads ved hjælp af en struktur kendt som en epiphragm. Sneglens slimede sekretion arbejder sig ind i porerne, der findes på selv tilsyneladende glatte overflader, derefter h
Ingeniører demonstrerer superstærk, vendbart klæbemiddel, der fungerer som snegleslime (opdaterin…Snegle kan forankre sig på plads ved hjælp af en struktur kendt som en epiphragm. Sneglens slimede sekretion arbejder sig ind i porerne, der findes på selv tilsyneladende glatte overflader, derefter h -
 Lysaktiveret metalkatalysator ødelægger kræftcellernes vitale energikildeKredit:University of Warwick Et metal i en rumalder, der var en del af asteroiden, der ødelagde dinosaurerne, kunne give en ny metode til selektiv behandling af kræfttumorer ved hjælp af lys. For
Lysaktiveret metalkatalysator ødelægger kræftcellernes vitale energikildeKredit:University of Warwick Et metal i en rumalder, der var en del af asteroiden, der ødelagde dinosaurerne, kunne give en ny metode til selektiv behandling af kræfttumorer ved hjælp af lys. For -
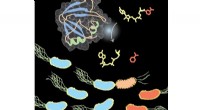 Ny indsigt i plantemikrobiomets molekylære våbenBilledet viser Tne2, et NAD-nedbrydende enzym udskilt gennem type 6 sekretionssystem af den plantebeskyttende bakterie Pseudomonas protegens. Kredit:John Whitney, McMaster University Som alle orga
Ny indsigt i plantemikrobiomets molekylære våbenBilledet viser Tne2, et NAD-nedbrydende enzym udskilt gennem type 6 sekretionssystem af den plantebeskyttende bakterie Pseudomonas protegens. Kredit:John Whitney, McMaster University Som alle orga
- Hvordan bevæger faste molekyler sig?
- Hvad er klassificeringen af løsninger efter faser?
- Tekstilfiberindlejret multiluminescerende enhed til fremtidige bærbare enheder
- Hvordan kan brug af elektricitet helbrede kroppen?
- En del af Stillehavet opvarmes ikke som forventet, købe hvorfor?
- Hvilken forbindelse indeholder både ioniske og kovalente bindinger En ammoniak B ammonium clhorid C…


