Ionledningsevne:Hvorfor leder opløste ioniske forbindelser elektricitet?
* Ioniske forbindelser: Disse forbindelser dannes af den elektrostatiske tiltrækning mellem positivt ladede ioner (kationer) og negativt ladede ioner (anioner). Tænk på dem som små magneter, der holdes sammen af modsatte ladninger.
* Opløser: Når en ionforbindelse opløses i et opløsningsmiddel som vand, trækker vandmolekylerne ionerne fra hinanden og bryder ionbindingerne. Disse ioner bliver omgivet af vandmolekyler (hydrering), som effektivt adskiller dem.
* Fri ioner: Nu er disse adskilte ioner frie til at bevæge sig rundt i opløsningen. De er ikke længere låst fast i en stiv krystalstruktur.
* Ledende elektricitet: Elektricitet er strømmen af ladede partikler. Når du anvender et elektrisk potentiale (spænding) over opløsningen, bevæger de frie ioner sig som reaktion på det elektriske felt. Positivt ladede ioner bevæger sig mod den negative elektrode (katode), og negativt ladede ioner bevæger sig mod den positive elektrode (anode). Denne strøm af ladede partikler udgør en elektrisk strøm, der gør opløsningen ledende.
Tænk på det sådan her: Forestil dig en flok mennesker, der står stille, de kan ikke let bevæge sig rundt. Forestil dig nu, at folkemængden spredes, og enkeltpersoner kan bevæge sig frit. Hvis du vil flytte noget gennem denne spredte skare, er det meget nemmere end at prøve at flytte det gennem den tætpakkede skare. På samme måde giver frie ioner i en opløsning mulighed for let strømning af elektricitet.
Vigtig bemærkning: Ioniske forbindelser leder kun elektricitet, når de er opløst i et opløsningsmiddel (som vand) eller når de er smeltede (smeltede). I deres faste tilstand er ionerne fikseret i et stift gitter, hvilket forhindrer dem i at bevæge sig frit, og derfor er de ikke ledende.
Sidste artikelKulstof og ilt:Forståelse af atomernes sammensætning
Næste artikelKlor og dioxid:Forståelse af kemiske forbindelser
 Varme artikler
Varme artikler
-
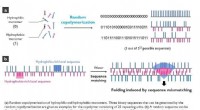 Ny polymer mesofasestruktur opdagetKredit:Korea Advanced Institute of Science and Technology Polymerer, store molekyler, der består af gentagne mindre molekyler kaldet monomerer, findes i næsten alt, hvad vi bruger i vores daglige l
Ny polymer mesofasestruktur opdagetKredit:Korea Advanced Institute of Science and Technology Polymerer, store molekyler, der består af gentagne mindre molekyler kaldet monomerer, findes i næsten alt, hvad vi bruger i vores daglige l -
 Forskere opdager metode til at kontrollere kræftfremkaldende formaldehydfrigivelse fra træ i hjemm…Kredit:Unsplash/CC0 Public Domain Ny forskning, ledet i fællesskab af University of Massachusetts Amherst og University of North Texas, fremmer vores forståelse af, hvordan træet i vores hjem og ko
Forskere opdager metode til at kontrollere kræftfremkaldende formaldehydfrigivelse fra træ i hjemm…Kredit:Unsplash/CC0 Public Domain Ny forskning, ledet i fællesskab af University of Massachusetts Amherst og University of North Texas, fremmer vores forståelse af, hvordan træet i vores hjem og ko -
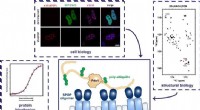 Hvordan ved et reguleringsprotein, hvor det skal bindes for at modulere insulinproduktionen?Penn State -forskere brugte en række forskellige teknikker vedrørende cellebiologi, strukturel biologi, og proteinbiofysik for at bestemme, hvordan proteinerne SPOP og Pdx1 fungerer sammen for at sikr
Hvordan ved et reguleringsprotein, hvor det skal bindes for at modulere insulinproduktionen?Penn State -forskere brugte en række forskellige teknikker vedrørende cellebiologi, strukturel biologi, og proteinbiofysik for at bestemme, hvordan proteinerne SPOP og Pdx1 fungerer sammen for at sikr -
 Molekylært stillads til modificering af fluorescerende forbindelser, der anvendes til biologisk bil…Et bibliotek af farvestofmolekyler syntetiseret med en modulær kemisk tilgang kan føre til forbedret billeddannelse af levende celler. Kredit:A*STAR Institute of Chemical and Engineering Sciences
Molekylært stillads til modificering af fluorescerende forbindelser, der anvendes til biologisk bil…Et bibliotek af farvestofmolekyler syntetiseret med en modulær kemisk tilgang kan føre til forbedret billeddannelse af levende celler. Kredit:A*STAR Institute of Chemical and Engineering Sciences
- Min undersøgelse viser, hvor hurtigt bakterier kan udvikle sig
- Hvorfor trives svampe uden at skade træerne, hvorfor det sker?
- Kaliumcarbonatdissociation:ligning, forklaring og opløselighed
- Hvad er de mest almindelige mineraler i Louisiana?
- Kinas miljødata:Verdens største forurener i antal
- Hjemmesiden vurderer sikkerheden for internet-tilsluttede enheder


