Periodiske tendenser:Forståelse af kemiske egenskabscyklusser
1. Elektronkonfiguration:
* Elektroner udfylder orbitaler i en bestemt rækkefølge: Når du bevæger dig hen over en periode, tilføjes protoner til kernen, og elektroner tilføjes til nye orbitaler.
* Lignende konfigurationer af yderste elektroner: Grundstoffer i samme gruppe (søjle) har det samme antal valenselektroner (elektroner i den yderste skal). Denne lignende ydre elektronkonfiguration er den primære årsag til deres lignende kemiske egenskaber.
2. Periodicitet:
* Fyldte og delvist fyldte skaller: Når du bevæger dig hen over en periode, fylder du gradvist den yderste elektronskal.
* Afskærmningseffekt: Når du bevæger dig ned ad en gruppe, øges antallet af indre elektronskaller, hvilket fører til en stærkere afskærmningseffekt. Det betyder, at de yderste elektroner er mindre tiltrukket af kernen, hvilket fører til større atomradier.
* Elektronegativitet: Elektronegativitet (et atoms tendens til at tiltrække elektroner) falder ned ad en gruppe på grund af afskærmningseffekten.
3. Gentagelse af kemiske egenskaber:
* Lignende reaktivitet: Grundstoffer med lignende elektronkonfigurationer udviser ofte lignende kemisk adfærd. For eksempel er alkalimetaller (Gruppe 1) meget reaktive på grund af deres enkeltvalenselektron, mens halogener (Gruppe 17) er reaktive, fordi de har brug for en elektron mere for at fuldende deres oktet.
* Tendenser i egenskaber: Når du bevæger dig gennem en periode, ser du mønstre i egenskaber som ioniseringsenergi (energi, der kræves for at fjerne en elektron), elektronaffinitet (tendens til at få en elektron) og metallisk karakter (evne til at miste elektroner).
* Kemisk binding: Grundstoffer i samme gruppe har tendens til at danne lignende typer bindinger med andre grundstoffer (f.eks. ionbindinger, kovalente bindinger).
Eksempel:
* Natrium (Na) og Kalium (K) , begge i gruppe 1, har en valenselektron og udviser lignende reaktivitet og danner ioniske forbindelser med halogener.
* Klor (Cl) og brom (Br) , begge i gruppe 17, har syv valenselektroner og reagerer på samme måde og danner ioniske forbindelser med alkalimetaller.
Opsummering: Den cykliske natur af kemiske egenskaber på tværs af perioder afspejler det grundlæggende princip, at elektronkonfiguration dikterer reaktivitet og andre kemiske egenskaber . Det er grunden til, at det periodiske system er så kraftfuldt til at forudsige og forstå grundstoffernes opførsel.
 Varme artikler
Varme artikler
-
 Forskere udvikler prober designet til at afsløre de fysiske kræfter inde i levende celler; en verd…Molekylær struktur af det kemiske værktøj (til venstre), blå:elektronfattig, rød:elektronrig, der ændrer farve som rejer under madlavning (midten, inspiration fra fiskemarkedet i Barcelona) for at afs
Forskere udvikler prober designet til at afsløre de fysiske kræfter inde i levende celler; en verd…Molekylær struktur af det kemiske værktøj (til venstre), blå:elektronfattig, rød:elektronrig, der ændrer farve som rejer under madlavning (midten, inspiration fra fiskemarkedet i Barcelona) for at afs -
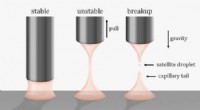 Et nyt twist til at bryde viskoelastiske væskebroerDen konventionelle metode til at bryde væskebroer bruger tilbagetrækning. Når dysen (eller pladen) løftes, væskebroen strækker sig og knækker. Dette kan danne kapillærhaler og satellitdråber. Forskere
Et nyt twist til at bryde viskoelastiske væskebroerDen konventionelle metode til at bryde væskebroer bruger tilbagetrækning. Når dysen (eller pladen) løftes, væskebroen strækker sig og knækker. Dette kan danne kapillærhaler og satellitdråber. Forskere -
 Hvordan katteurt gør det kemikalie, der får katte til at gå amokKattenip har en velkendt effekt på, dets berusende højder er forårsaget af nepetalactone, en type kemikalie kaldet terpen. Kredit:John Innes Center Forskere ved John Innes Center har kastet lys ov
Hvordan katteurt gør det kemikalie, der får katte til at gå amokKattenip har en velkendt effekt på, dets berusende højder er forårsaget af nepetalactone, en type kemikalie kaldet terpen. Kredit:John Innes Center Forskere ved John Innes Center har kastet lys ov -
 Nye fund om den største naturlige svovlkilde i atmosfærenLaboratorieopsætning af gratis jet-eksperimentet på TROPOS i Leipzig, som muliggør undersøgelse af den tidlige fase af oxidationsreaktioner under atmosfæriske forhold uden at væggene påvirker reaktion
Nye fund om den største naturlige svovlkilde i atmosfærenLaboratorieopsætning af gratis jet-eksperimentet på TROPOS i Leipzig, som muliggør undersøgelse af den tidlige fase af oxidationsreaktioner under atmosfæriske forhold uden at væggene påvirker reaktion
- Er gravitationsenergi en vedvarende kilde eller kilde?
- Forskere afslører, hvad der får planter til at størkne
- Hvorfor bruges talkum til at reducere friktion med eksempler?
- Hvad er dagligdags genstande, der reflekterer alle farverne i sollys?
- Hvorfor stjerner varierer i farve?
- 1 liter i minuttet så hvor mange gallon uge?


