Magnesium og ilt:Forståelse af ionisk bindingsdannelse
* Elektronegativitet: Elektronegativitet er et atoms evne til at tiltrække elektroner mod sig selv i en kemisk binding. Oxygen har en høj elektronegativitet (3,44), mens magnesium har en lav elektronegativitet (1,31).
* Elektronoverførsel: Den store elektronegativitetsforskel betyder, at ilt har et meget stærkere træk på elektroner end magnesium. Når de interagerer, "stjæler" oxygen effektivt to elektroner fra magnesium.
* Danning af ioner: Magnesium, der har mistet to elektroner, bliver en positivt ladet ion (Mg²⁺). Ilt, der har fået to elektroner, bliver en negativt ladet ion (O²⁻).
* Elektrostatisk tiltrækning: Disse modsat ladede ioner holdes derefter sammen af en stærk elektrostatisk tiltrækning, der danner den ioniske binding, der udgør magnesiumoxid (MgO).
Opsummering: Den betydelige elektronegativitetsforskel mellem magnesium og oxygen driver overførslen af elektroner, hvilket fører til dannelsen af ladede ioner og den elektrostatiske tiltrækning, der definerer en ionbinding.
 Varme artikler
Varme artikler
-
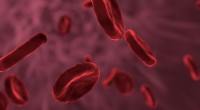 Ny enhed identificerer bloddonorer af høj kvalitetKredit:CC0 Public Domain Blodbanker har længe kendt til donorer af høj kvalitet - individer, hvis røde blodlegemer forbliver levedygtige i længere tid i opbevaring og i modtagerens krop. Nu viser
Ny enhed identificerer bloddonorer af høj kvalitetKredit:CC0 Public Domain Blodbanker har længe kendt til donorer af høj kvalitet - individer, hvis røde blodlegemer forbliver levedygtige i længere tid i opbevaring og i modtagerens krop. Nu viser -
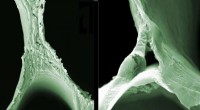 Generering af elektricitet gennem gulvoverfladerScanning elektronmikroskopi (SEM) billeder af balsa træ (venstre) og delignificeret træ illustrerer de strukturelle ændringer. Kredit:ACS Nano / Empa Ingo Burgert og hans team hos Empa og ETH Züri
Generering af elektricitet gennem gulvoverfladerScanning elektronmikroskopi (SEM) billeder af balsa træ (venstre) og delignificeret træ illustrerer de strukturelle ændringer. Kredit:ACS Nano / Empa Ingo Burgert og hans team hos Empa og ETH Züri -
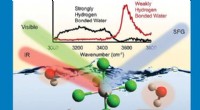 Unik grænseflade og uventet adfærd hjælper med at forklare, hvordan tungmetaller virkerForskere identificerede tre forskellige typer vandmolekyler, der omgiver en tung, anionisk metalchloridkompleks (nederst) ved brug af spektroskopi (øverst) ved en luft/vand-grænseflade. Hver type vand
Unik grænseflade og uventet adfærd hjælper med at forklare, hvordan tungmetaller virkerForskere identificerede tre forskellige typer vandmolekyler, der omgiver en tung, anionisk metalchloridkompleks (nederst) ved brug af spektroskopi (øverst) ved en luft/vand-grænseflade. Hver type vand -
 Kunstig intelligens ARTIST fanger øjeblikkeligt materialeegenskaberKUNSTNER, som står for Artificial Intelligence for Spectroscopy, bestemmer øjeblikkeligt, hvordan et molekyle vil reagere på lys. Kredit:Jari Järvi/Aalto University Forskere ved Aalto Universitet
Kunstig intelligens ARTIST fanger øjeblikkeligt materialeegenskaberKUNSTNER, som står for Artificial Intelligence for Spectroscopy, bestemmer øjeblikkeligt, hvordan et molekyle vil reagere på lys. Kredit:Jari Järvi/Aalto University Forskere ved Aalto Universitet
- Netflix-abonnenter dropper hints om streaming-tjenestetræthed
- Hvad er symbolet for forskydning i videnskaben?
- Udvikling af det hurtigste og mest følsomme grafenmikrobølgebolometer
- Spinner jorden rundt om sol eller måne?
- Påvirker aminosyrer proteinfunktioner?
- Hvor meget elektricitet bruger en menneskelig brug om dagen?


