Ester vs. Carboxylsyre kogepunkter:Forstå forskellen
1. Mangel på hydrogenbinding:
* Carboxylsyrer danner stærke hydrogenbindinger med hinanden på grund af tilstedeværelsen af det sure brintatom. Disse brintbindinger kræver betydelig energi for at bryde, hvilket fører til højere kogepunkter.
* Estere mangler det sure brintatom, så de kan kun danne svage dipol-dipol-vekselvirkninger. Disse interaktioner er meget svagere end hydrogenbindinger, hvilket resulterer i lavere kogepunkter.
2. Reduceret polaritet:
* Carboxylsyrer har en højere polaritet end estere på grund af tilstedeværelsen af den polære hydroxylgruppe (-OH). Denne højere polaritet bidrager yderligere til stærkere intermolekylære kræfter og højere kogepunkter.
* Estere har en mindre polær struktur, hvor oxygenatomet i carbonylgruppen (C=O) er mindre elektronegativt end oxygenet i hydroxylgruppen af carboxylsyrer. Dette reducerer styrken af dipol-dipol-interaktioner og resulterer i lavere kogepunkter.
3. Molekylvægt:
* Selvom det ikke er den primære årsag, er esteres molekylvægt typisk lidt lavere end deres tilsvarende carboxylsyrer. Denne mindre molekylvægt bidrager lidt til det lavere kogepunkt for estere.
Opsummering:
Manglen på hydrogenbinding og reduceret polaritet i estere sammenlignet med carboxylsyrer er hovedårsagerne til deres lavere kogepunkter. Disse faktorer reducerer betydeligt styrken af intermolekylære kræfter, hvilket gør det lettere at fordampe estere.
 Varme artikler
Varme artikler
-
 Video:Kan blanding af husholdningsrengøringsmidler dræbe dig?Kredit:The American Chemical Society Når badeværelset begynder at se grimt ud, og det er tid til at piske gule handsker frem, det eneste, der betyder noget, er at få arbejdet udført hurtigt. Så d
Video:Kan blanding af husholdningsrengøringsmidler dræbe dig?Kredit:The American Chemical Society Når badeværelset begynder at se grimt ud, og det er tid til at piske gule handsker frem, det eneste, der betyder noget, er at få arbejdet udført hurtigt. Så d -
 Kemiprofessor bruger gamle materialer til at lave nyere, bedre solcellerBiwu Ma, professor i kemi og biokemi, offentliggjort en ny undersøgelse om, hvordan en ny struktur kunne skabe blåt lys i en type materiale kaldet en perovskit. Kredit:Florida State University Et
Kemiprofessor bruger gamle materialer til at lave nyere, bedre solcellerBiwu Ma, professor i kemi og biokemi, offentliggjort en ny undersøgelse om, hvordan en ny struktur kunne skabe blåt lys i en type materiale kaldet en perovskit. Kredit:Florida State University Et -
 Ny dobbelt-atom katalysator viser løfte om at give ren energi ved kunstig fotosynteseEn strukturel karakterisering af en ny iridium dinukleær heterogen katalysator afslører lyse par af atomer. Den nye katalysator betragtes som et fremskridt i bestræbelserne på at producere og lagre re
Ny dobbelt-atom katalysator viser løfte om at give ren energi ved kunstig fotosynteseEn strukturel karakterisering af en ny iridium dinukleær heterogen katalysator afslører lyse par af atomer. Den nye katalysator betragtes som et fremskridt i bestræbelserne på at producere og lagre re -
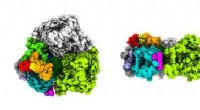 Unikke pigmenter i fotosyntetiske marinebakterier afslører, hvordan den lever i svagt lysFigur 1:Et kryo-elektronmikroskopi tæthedskort over Acaryochloris marina fotosystem I afslører strukturelle elementer, der gør det muligt for det at omdanne lavenergilys til kemisk energi. Kredit:Æn
Unikke pigmenter i fotosyntetiske marinebakterier afslører, hvordan den lever i svagt lysFigur 1:Et kryo-elektronmikroskopi tæthedskort over Acaryochloris marina fotosystem I afslører strukturelle elementer, der gør det muligt for det at omdanne lavenergilys til kemisk energi. Kredit:Æn
- Nye metoder hjælper med at identificere, hvad der driver følsom eller socialt uacceptabel adfærd
- Videnskaben siger:Hvorfor nogle flyvemaskiner ikke flyver i høj varme
- Ny patenteret opfindelse stabiliserer, roterer satellitter
- Hvad er komponenterne i et økosystem?
- Hvad er de kinetiske molekylære teori -effekter på tryk og volumen af gasprøve?
- Hvorfor det er så svært at forudsige sne i Storbritannien


