Hvad er de kinetiske molekylære teori -effekter på tryk og volumen af gasprøve?
1. gasmolekyler er i konstant, tilfældig bevægelse. Dette betyder, at de konstant kolliderer med hinanden og med væggene i deres beholder.
2. gasmolekyler er meget små sammenlignet med afstandene mellem dem. Dette betyder, at volumenet af selve gasmolekylerne er ubetydelig sammenlignet med volumenet af den beholder, de optager.
3. gasmolekyler har ingen attraktive eller frastødende kræfter mellem dem. Dette betyder, at de bevæger sig uafhængigt af hinanden.
4. Kollisioner mellem gasmolekyler er perfekt elastiske. Dette betyder, at der ikke er noget tab af energi under kollisioner.
5. Den gennemsnitlige kinetiske energi af gasmolekyler er proportional med den absolutte temperatur. Dette betyder, at når temperaturen stiger, øges gasmolekylernes gennemsnitlige hastighed.
Sådan påvirker disse postulater tryk og volumen:
tryk:
* tryk er forårsaget af kollisioner af gasmolekyler med vægge i beholderen. Jo hyppigere og kraftfulde kollisioner, jo højere er trykket.
* Forøgelse af temperaturen på en gas øger den gennemsnitlige kinetiske energi for molekylerne, hvilket fører til hyppigere og kraftfulde kollisioner. Derfor øges trykket med stigende temperatur.
* Faldende volumen af en beholder tvinger molekylerne til at kollidere oftere med væggene. Dette øger presset.
bind:
* Mængden af en gas bestemmes af det rum, den optager i en beholder.
* Forøgelse af temperaturen på en gas får molekylerne til at bevæge sig hurtigere og kollidere oftere med væggene. For at opretholde det samme tryk skal beholderens volumen stige.
* Faldende volumen af en beholder tvinger molekylerne til at kollidere oftere med væggene. Dette øger trykket, hvilket kan modvirkes ved at reducere temperaturen for at reducere molekylernes kinetiske energi.
Nøgleforhold:
* Boyle's lov: Ved konstant temperatur er volumenet af en gas omvendt proportional med dens tryk (V ∝ 1/P).
* Charles 'lov: Ved konstant tryk er volumenet af en gas direkte proportional med dens absolutte temperatur (V ∝ T).
* Gay-Lussacs lov: Ved konstant volumen er trykket fra en gas direkte proportionalt med dens absolutte temperatur (P ∝ T).
Kortfattet:
Den kinetiske molekylære teori forklarer, hvordan opførslen af gasmolekyler påvirker tryk og volumen. Når hastigheden og hyppigheden af kollisioner stiger (på grund af øget temperatur eller nedsat volumen) stiger trykket. Omvendt muliggør øget volumen ved konstant temperatur færre kollisioner, hvilket reducerer trykket. Disse forhold danner grundlaget for den ideelle gaslov, der kombinerer Boyle's, Charles's og Gay-Lussacs love for at beskrive gassens opførsel under forskellige forhold.
 Varme artikler
Varme artikler
-
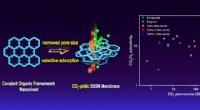 Enfasede kovalente organiske rammemembraner gør CO2-selektiv separation muligIllustration af overlegen CO2-selektiv COF nanosheet membran til højtydende CO2/H2 separation. Kredit:Peng Yuan En forskningsgruppe ledet af prof. Yang Weishen og Dr. Peng Yuan fra Dalian Institut
Enfasede kovalente organiske rammemembraner gør CO2-selektiv separation muligIllustration af overlegen CO2-selektiv COF nanosheet membran til højtydende CO2/H2 separation. Kredit:Peng Yuan En forskningsgruppe ledet af prof. Yang Weishen og Dr. Peng Yuan fra Dalian Institut -
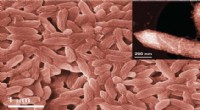 Rekruttering af bakterier til at bygge katalysatorer atom for atomForskerholdet udnyttede den jernåndende bakterie Geobacter sulfurreducens til at syntetisere enkeltatom-katalysatorer, som kan bruges til forskellige energirelaterede applikationer. Kredit:KAUST U
Rekruttering af bakterier til at bygge katalysatorer atom for atomForskerholdet udnyttede den jernåndende bakterie Geobacter sulfurreducens til at syntetisere enkeltatom-katalysatorer, som kan bruges til forskellige energirelaterede applikationer. Kredit:KAUST U -
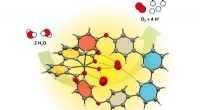 Kunstigt enzym opdeler vand mere effektivtEnzymlignende vandfororganisering foran en Ruthenium-vandoxidationskatalysator. Kredit:Würthner-gruppen / Würzburg Universitet Menneskeheden står over for en central udfordring:Den skal klare overg
Kunstigt enzym opdeler vand mere effektivtEnzymlignende vandfororganisering foran en Ruthenium-vandoxidationskatalysator. Kredit:Würthner-gruppen / Würzburg Universitet Menneskeheden står over for en central udfordring:Den skal klare overg -
 Enkel, billig metode til at beskytte kulfiberYongfeng Lu. Kredit:Craig Chandler | Universitetskommunikation I de sidste 50 år, producenter har betragtet kulfiber som et drømmemateriale:Selvom individuelle fibre er tyndere end et hårstrå, de
Enkel, billig metode til at beskytte kulfiberYongfeng Lu. Kredit:Craig Chandler | Universitetskommunikation I de sidste 50 år, producenter har betragtet kulfiber som et drømmemateriale:Selvom individuelle fibre er tyndere end et hårstrå, de
- Californiens regntid er her. Hvad betyder det for vandforsyningen?
- Hvorfor er det fornuftigt på diagrammer at repræsentere en kraft ved en pil?
- Hvad er metoderne til formeltransformation?
- Hvad er nogle fordele og ulemper ved klart skæring?
- Hvad er spin degeneration?
- Teoretisk undersøgelse viser, at stof har en tendens til at blive ordnet ved lave temperaturer


