Zink kan fortrænge kobber fra sulfatopløsning, fordi zink er?
Her er hvorfor:
* reaktivitetsserien: Metaller er arrangeret i en reaktivitetsserie baseret på deres tendens til at miste elektroner og danne positive ioner. Metaller, der er højere i serien, er mere reaktive end dem, der er lavere i serien.
* forskydningsreaktioner: I en forskydningsreaktion vil et mere reaktivt metal fortrænge et mindre reaktivt metal fra dets forbindelse.
* zink og kobber: Zink er højere i reaktivitetsserien end kobber. Dette betyder, at zink har en stærkere tendens til at miste elektroner og danne positive ioner (Zn²⁺). Når zink tilsættes til en kobbersulfatopløsning (CUSO₄), mister zinkatomer let elektroner og danner zinkioner (Zn²⁺). Disse ioner kombineres derefter med sulfationerne (SO₄²⁻) for at danne zinksulfat (ZnSO₄). På samme tid forskydes kobberioner (Cu²⁺) fra opløsningen og danner fast kobbermetal.
Den kemiske ligning for reaktionen er:
Zn (s) + cuso₄ (aq) → Znso₄ (aq) + cu (s)
 Varme artikler
Varme artikler
-
 Verdens første til at læse digitalt kodede syntetiske molekylerVed at indsætte skrøbelige bindinger mellem hver molekylær byte, digitale polymerer kan let aflæses gennem massespektrometri. Kredit:Jean-François Lutz, Institut Charles Sadron (CNRS) Ved hjælp af
Verdens første til at læse digitalt kodede syntetiske molekylerVed at indsætte skrøbelige bindinger mellem hver molekylær byte, digitale polymerer kan let aflæses gennem massespektrometri. Kredit:Jean-François Lutz, Institut Charles Sadron (CNRS) Ved hjælp af -
 Stor dråbesortering nu mulig ved høje hastighederBioingeniører fra UCLA og University of Tokyo har øget den hastighed, hvormed store væskedråber, potentielt indeholdende individuelle levende celler, kan sorteres intakt og i løs vægt. Ifølge forskni
Stor dråbesortering nu mulig ved høje hastighederBioingeniører fra UCLA og University of Tokyo har øget den hastighed, hvormed store væskedråber, potentielt indeholdende individuelle levende celler, kan sorteres intakt og i løs vægt. Ifølge forskni -
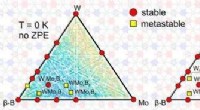 Forskere forudsiger nyt, hårdt, og superhårde ternære forbindelserTernær fasediagram over W-Mo-B-systemet ved 0 K. Kredit:A. Kvashnin et al./Chemistry of Materials Forskere fra Skolkovo Institute of Science and Technology (Skoltech), Institute of Solid State Che
Forskere forudsiger nyt, hårdt, og superhårde ternære forbindelserTernær fasediagram over W-Mo-B-systemet ved 0 K. Kredit:A. Kvashnin et al./Chemistry of Materials Forskere fra Skolkovo Institute of Science and Technology (Skoltech), Institute of Solid State Che -
 Havpattedyrs tilpasninger til lavt ilt giver et nyt perspektiv på COVID-19Kredit:CC0 Public Domain Da Terrie Williams begyndte at høre om den brede vifte af symptomer, som patienter med COVID-19 oplevede, hun så en sammenhæng mellem de forskellige måder sygdommen påvirk
Havpattedyrs tilpasninger til lavt ilt giver et nyt perspektiv på COVID-19Kredit:CC0 Public Domain Da Terrie Williams begyndte at høre om den brede vifte af symptomer, som patienter med COVID-19 oplevede, hun så en sammenhæng mellem de forskellige måder sygdommen påvirk
- Tørke på Afrikas Horn:Forskning viser, hvordan et netværk af grundvandsboringer kunne hjælpe
- Rekordstor solcelle annonceret af multinationalt forskerhold
- Adskillelse en sød succes
- At sænke farten kan forhindre for tidlig udbrændthed af McDonaldiserede virksomheder og personale
- Eksempler på sekundære forurenende stoffer
- Bekostelig gasseparation er muligvis ikke nødvendig for at genanvende CO₂ fra luft og industrianlæ…


