Vandopløselige molekylære forbindelser og elektrisk ledningsevne:Forståelse af sammenhængen
Her er hvorfor:
* Molekylære forbindelser dannes ved deling af elektroner mellem atomer (kovalente bindinger).
* Vand er et polært opløsningsmiddel, hvilket betyder, at det har en positiv og negativ ende på grund af ujævn deling af elektroner i O-H-bindingerne.
* Nogle molekylære forbindelser opløses i vand fordi de polære vandmolekyler kan omgive og interagere med forbindelsens molekyler og trække dem fra hinanden.
* Ikke alle molekylære forbindelser opløses i vand . En forbindelses evne til at opløse afhænger af styrken af tiltrækningen mellem vandmolekylerne og forbindelsens molekyler.
* Nogle molekylære forbindelser, der opløses i vand, kan lede elektricitet fordi de ioniserer i opløsning. Det betyder, at de går fra hinanden til ladede ioner (kationer og anioner). Disse ioner er frie til at bevæge sig og bære en elektrisk strøm.
Eksempler:
* Sukker (saccharose) er en molekylær forbindelse, der opløses i vand, men ikke gør det lede elektricitet, fordi det ikke ioniserer.
* Saltsyre (HCl) er en molekylær forbindelse, der opløses i vand og leder elektricitet fordi det ioniseres til H+ og Cl- ioner.
Nøgleafhentning: Om en molekylær forbindelse leder elektricitet i vand afhænger af, om den ioniserer, ikke kun af, om den opløses.
 Varme artikler
Varme artikler
-
 Pig-Pen-effekt:Blanding af hudolie og ozon kan producere en personlig forureningsskyNår ozon rammer olier på huden og i snavset tøj, det kan producere en personlig sky af irriterende stoffer. Kredit:Penn State Når ozon og hudolier mødes, den resulterende reaktion kan hjælpe med a
Pig-Pen-effekt:Blanding af hudolie og ozon kan producere en personlig forureningsskyNår ozon rammer olier på huden og i snavset tøj, det kan producere en personlig sky af irriterende stoffer. Kredit:Penn State Når ozon og hudolier mødes, den resulterende reaktion kan hjælpe med a -
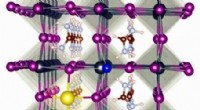 Et komplet sæt energiniveaupositioner for alle primære metalhalogenidperovskitterKredit:Eindhoven University of Technology Metalhalogenidperovskitter udgør en populær klasse af materialer med spændende optoelektroniske egenskaber. En grundlæggende forståelse af variationerne i
Et komplet sæt energiniveaupositioner for alle primære metalhalogenidperovskitterKredit:Eindhoven University of Technology Metalhalogenidperovskitter udgør en populær klasse af materialer med spændende optoelektroniske egenskaber. En grundlæggende forståelse af variationerne i -
 Alger som levende biokatalysatorer for en grøn industriKredit:CC0 Public Domain Mange stoffer, som vi bruger hver dag, virker kun i den rigtige 3-D struktur. Naturlige enzymer kunne producere disse på en miljøvenlig måde - hvis de ikke havde brug for
Alger som levende biokatalysatorer for en grøn industriKredit:CC0 Public Domain Mange stoffer, som vi bruger hver dag, virker kun i den rigtige 3-D struktur. Naturlige enzymer kunne producere disse på en miljøvenlig måde - hvis de ikke havde brug for -
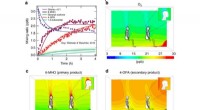
 Foto-induceret ionforskydning i blandede halogenidperovskitter til et batteri, der kan oplades direk…PL-emissionskortlægning af MA0.17FA0.83Pb(I0.5Br0.5)3 ved detektionsbølgelængden på 670 nm og 790 nm efter lokal belysning i 1 time med en strålestørrelse på ~ 1 mm og tæthed på 1 sol på den bare film
Foto-induceret ionforskydning i blandede halogenidperovskitter til et batteri, der kan oplades direk…PL-emissionskortlægning af MA0.17FA0.83Pb(I0.5Br0.5)3 ved detektionsbølgelængden på 670 nm og 790 nm efter lokal belysning i 1 time med en strålestørrelse på ~ 1 mm og tæthed på 1 sol på den bare film
- Hvad der sker, når temperaturen på et stof falder markant A. De fleste stoffer vil ekspandere. B. …
- Hvorfor et udkast ville svække det amerikanske militær
- Team rapporterer skalerbar fremstilling af selvjusterede grafentransistorer, kredsløb
- Hvordan beregner du hastigheden på nogen planet?
- Hvad er Blood Agar Tellurite Medium?
- Strenge adgangskodepolitikker hjælper med at forhindre svindel, undersøgelse finder


