Forståelse af kemiske reaktioner:Hvordan atomer binder
1. Elektronkonfiguration:
* Valenselektroner: De yderste elektroner i et atom kaldes valenselektroner. Det er dem, der er involveret i kemisk binding.
* Oktetregel: De fleste atomer stræber efter at opnå en stabil elektronkonfiguration som for en ædelgas (gruppe 18 i det periodiske system), som typisk har otte elektroner i deres yderste skal (undtagen helium, som har to). Dette er kendt som oktetreglen.
2. Elektronegativitet:
* Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner i en kemisk binding.
* Atomer med højere elektronegativitet har tendens til at tiltrække elektroner stærkere. Dette påvirker typen af dannet binding:
* ioniske bindinger: Dannes, når der er stor forskel i elektronegativitet mellem to atomer. Det ene atom "donerer" effektivt en elektron til det andet og skaber ioner med modsatte ladninger, der tiltrækker hinanden.
* Kovalente bindinger: Opstår når atomer deler elektroner. Delingen kan være ens (ikke-polær kovalent binding) eller ulige (polær kovalent binding) afhængigt af elektronegativitetsforskellen.
3. Ioniseringsenergi:
* Ioniseringsenergi er den energi, der kræves for at fjerne en elektron fra et atom.
* Atomer med lavere ioniseringsenergi har en tendens til lettere at miste elektroner og danner ofte kationer (positivt ladede ioner).
4. Elektronaffinitet:
* Elektronaffinitet er ændringen i energi, når en elektron føjes til et neutralt atom for at danne en negativ ion (anion).
* Atomer med høj elektronaffinitet får let elektroner.
5. Atomstørrelse:
* Atomstørrelse spiller en rolle for, hvor let et atom kan interagere med andre atomer. Større atomer har mere løst fastholdte elektroner, hvilket gør dem mere tilbøjelige til at danne bindinger.
6. Andre faktorer:
* Atomladning: Antallet af protoner i et atoms kerne påvirker dets tiltrækning til elektroner.
* Afskærmningseffekt: De indre elektroner "skærmer" de ydre elektroner fra den fulde nukleare ladning, hvilket gør dem nemmere at fjerne.
Opsummering:
Den måde, atomer reagerer på, er et komplekst samspil mellem disse faktorer. At forstå elektronkonfigurationen og egenskaberne som elektronegativitet, ioniseringsenergi og elektronaffinitet hjælper med at forudsige, hvilken type binding et atom vil danne, og hvordan det vil interagere med andre atomer.
 Varme artikler
Varme artikler
-
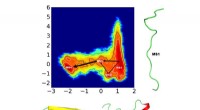 Ny metode fremskynder simuleringer, giver ny indsigt i proteinfoldningForskere søger at forstå proteinfoldning bedre for at helbrede fejlfoldningssygdomme, men denne utroligt komplekse proces kræver sofistikerede algoritmer til at identificere foldemekanismerne. Beregni
Ny metode fremskynder simuleringer, giver ny indsigt i proteinfoldningForskere søger at forstå proteinfoldning bedre for at helbrede fejlfoldningssygdomme, men denne utroligt komplekse proces kræver sofistikerede algoritmer til at identificere foldemekanismerne. Beregni -
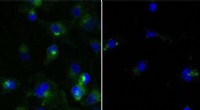 Cellulær oprydning kan også feje former for kræft vækCeller ubehandlet (venstre) eller behandlet (højre) med en PROTAC, der nedbryder målproteinet (grønt). Kredit:Yale University To nye forskningsartikler forstærker fordelene ved en ny terapi, der k
Cellulær oprydning kan også feje former for kræft vækCeller ubehandlet (venstre) eller behandlet (højre) med en PROTAC, der nedbryder målproteinet (grønt). Kredit:Yale University To nye forskningsartikler forstærker fordelene ved en ny terapi, der k -
 Beton med forbedret slagfasthed til forsvarsstrukturerKredit:FEFU Ingeniører fra Center for Militære Studier ved Far Eastern Federal University (MSC FEFU) udviklede beton med forbedret slagfasthed og fremstillet af op til 40 procent affald fra risska
Beton med forbedret slagfasthed til forsvarsstrukturerKredit:FEFU Ingeniører fra Center for Militære Studier ved Far Eastern Federal University (MSC FEFU) udviklede beton med forbedret slagfasthed og fremstillet af op til 40 procent affald fra risska -
 Forskere tvivler på, at DeepMinds AI er så god til systemer med fraktioneret opladning, som det se…Forholdet mellem BBB-testsystemerne og fraktionelle ladningsatomer fra træningssættet. Kredit:Michael Medvedev (Zelinsky Institute of Organic Chemistry of RAS) I deres papir offentliggjort i Scienc
Forskere tvivler på, at DeepMinds AI er så god til systemer med fraktioneret opladning, som det se…Forholdet mellem BBB-testsystemerne og fraktionelle ladningsatomer fra træningssættet. Kredit:Michael Medvedev (Zelinsky Institute of Organic Chemistry of RAS) I deres papir offentliggjort i Scienc
- Hvad er nogle fordele og ulemper ved at bruge vindenergi til at skabe elektricitet?
- Hvorfor fungerer vira som en parasit og finder værtscelle?
- Hvilken slags potentiel energi har olie?
- Hvorfor er fortyndet natriumhydrogencarbonatopløsning, der bruges i et bægerglas, når man laver e…
- Hvad sker der, når du sætter evolution på replay?
- En ny (mikro) linse om optik:Forskere udvikler hybride achromater med høj fokuseringseffektivitet


