pH af vand ved 70°C:Beregning og forståelse
Forstå pH og temperatur
* pH: Et mål for surhedsgraden eller alkaliniteten af en opløsning. Det er baseret på koncentrationen af hydrogenioner (H+).
* Temperatur: Når temperaturen stiger, øges dissociationen af vandmolekyler (H2O → H+ + OH-). Dette betyder, at der er flere hydrogenioner (H+) til stede, hvilket fører til en lavere pH (mere sur).
Beregning
1. Ionprodukt af vand (Kw): Ved 25°C er Kw 1,0 x 10^-14. Kw ændres dog med temperaturen.
2. Kw ved 70°C: Du skal bruge en tabel eller en ligning for at finde Kw-værdien ved 70°C. Værdien er cirka 2,5 x 10^-13.
3. Beregn H+-koncentration:
* Kw =[H+][OH-]
* Da rent vand har lige store koncentrationer af H+ og OH-, kan vi simplificere til:Kw =[H+]^2
* [H+] =√Kw =√(2,5 x 10^-13) ≈ 5,0 x 10^-7 M
4. pH-beregning:
* pH =-log[H+]
* pH =-log(5,0 x 10^-7) ≈ 6,3
Resultat: pH-værdien af rent vand ved 70°C er ca. 6,3 .
Vigtig bemærkning: Selvom pH er lidt lavere end 7, betragtes rent vand ved 70°C stadig som neutralt, fordi koncentrationerne af H+ og OH- er lige store.
 Varme artikler
Varme artikler
-
 Forskere producerer robust katalysator til at spalte vand til brint, iltEn katalysator udviklet af Rice University og University of Houston opdeler vand til brint og oxygen uden behov for dyre metaller som platin. Dette elektronmikroskopbillede viser nikkelskum belagt med
Forskere producerer robust katalysator til at spalte vand til brint, iltEn katalysator udviklet af Rice University og University of Houston opdeler vand til brint og oxygen uden behov for dyre metaller som platin. Dette elektronmikroskopbillede viser nikkelskum belagt med -
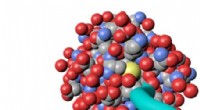 Miami kemis gennembrudsteknik muliggør design i grænsefladen mellem kemi og biologiEn syntetisk polymer (teal tube) konjugeret til et protein. Den lilla muffe på polymeren er en rapporteringsgruppe, nøglen til Konkolewicz og Pages teknik. Kredit:Miami University En teknik udvikl
Miami kemis gennembrudsteknik muliggør design i grænsefladen mellem kemi og biologiEn syntetisk polymer (teal tube) konjugeret til et protein. Den lilla muffe på polymeren er en rapporteringsgruppe, nøglen til Konkolewicz og Pages teknik. Kredit:Miami University En teknik udvikl -
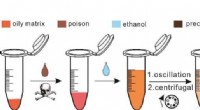 Ethanol-ekstraktion SERS-strategi giver meget følsom påvisning af giftstoffer i olieagtig matrixSkematisk diagram af SERS-detektion baseret på ethanolekstraktion. Kredit:WANG Yongtao Forskere fra det kinesiske videnskabsakademi (CAS) udviklede for nylig en ethanol-ekstraktionsoverfladeforstæ
Ethanol-ekstraktion SERS-strategi giver meget følsom påvisning af giftstoffer i olieagtig matrixSkematisk diagram af SERS-detektion baseret på ethanolekstraktion. Kredit:WANG Yongtao Forskere fra det kinesiske videnskabsakademi (CAS) udviklede for nylig en ethanol-ekstraktionsoverfladeforstæ -
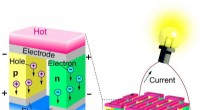 Flere halvleder type switch til at øge termoelektrisk konvertering af spildvarmeTinmonoselenid (SnSe), når dopet med antimon (Sb), kan danne en egnet kandidat til design af termoelektriske konverteringselementer (p-n-forbindelsesenhed). Kredit:Tokyo Tech I de seneste år, ener
Flere halvleder type switch til at øge termoelektrisk konvertering af spildvarmeTinmonoselenid (SnSe), når dopet med antimon (Sb), kan danne en egnet kandidat til design af termoelektriske konverteringselementer (p-n-forbindelsesenhed). Kredit:Tokyo Tech I de seneste år, ener


